Ανακοινώθηκαν θετικά αποτελέσματα από την κλινική μελέτη Φάσης 3 CAFÉ του dupilumab σε ενήλικες με μέτρια έως σοβαρή ατοπική δερματίτιδα (ΑΔ) οι οποίοι δεν ελέγχονται επαρκώς ή παρουσιάζουν δυσανεξία στο ευρέως χρησιμοποιούμενο ανοσοκατασταλτικό φάρμακο, κυκλοσπορίνη Α (CSA), ή όταν η συγκεκριμένη θεραπεία δεν ενδείκνυται. Στη μελέτη, το dupilumab με τοπικά κορτικοστεροειδή (TCS) βελτίωσε σημαντικά παραμέτρους που σχετίζονται με τη συνολική βαρύτητα της νόσου, την κάθαρση του δέρματος, τον κνησμό καθώς και παραμέτρους που αφορούν στην αναφερόμενη από τον ασθενή ποιότητα ζωής. Η κυκλοσπορίνη Α (CSA) είναι εγκεκριμένη για τη θεραπεία της Ατοπικής Δερματίτιδας (ΑΔ) στις περισσότερες ευρωπαϊκές χώρες και την Ιαπωνία· δεν έχει λάβει έγκριση στις ΗΠΑ για τη συγκεκριμένη χρήση. Τα αποτελέσματα αυτής της μελέτης παρουσιάστηκαν στο συνέδριο της Ευρωπαϊκής Ακαδημίας Δερματολογίας και Αφροδισιολογίας (EADV) στη Γενεύη της Ελβετίας.
Το πρωτεύον καταληκτικό σημείο της μελέτης ήταν το ποσοστό των ασθενών που πέτυχαν βελτίωση κατά 75% ή υψηλότερη βάση του δείκτη EASI-75 (Eczema Area and Severity Index/Δείκτης Έκτασης και Βαρύτητας του Εκζέματος) τη 16η εβδομάδα από την έναρξη της μελέτης. Ο δείκτης EASI αποτελεί ένα εργαλείο που χρησιμοποιείται για τον υπολογισμό της έκτασης και της βαρύτητας της νόσου. Το 59% των ασθενών που έλαβαν dupilumab εβδομαδιαίως σε συνδυασμό με τοπικά κορτικοστεροειδή και το 63% των ασθενών που έλαβαν dupilumab κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν EASI-75, σε σύγκριση με το 30% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p μικρότερο από 0,0001).
Η μέση ποσοστιαία μεταβολή που αφορά στη βελτίωση βάσει του δείκτη EASI από την έναρξη της μελέτης έως τη 16η εβδομάδα (ένα δευτερεύον καταληκτικό σημείο) ήταν 78% και 80% για τους ασθενείς που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή (TCS), αντίστοιχα, σε σύγκριση με το 47% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p μικρότερο από 0,0001).
"Στη μέτρια έως σοβαρή ατοπική δερματίτιδα, ορισμένοι ασθενείς είτε διακόπτουν τη θεραπευτική αγωγή με κυκλοσπορίνη εξαιτίας μη ανοχής ή έλλειψης αποτελεσματικότητας είτε δεν είναι κατάλληλοι για τη θεραπεία εξαιτίας άλλων ιατρικών παθήσεων ή αντενδείξεων," δήλωσε η Dr. Marjolein De Bruin-Weller, Dermatologist, National Expertise Center for Atopic Dermatitis, University Medical Center Utrecht. "Στη μελέτη CAFÉ, το dupilumab σε συνδυασμό με τοπικά κορτικοστεροειδή βελτίωσε σημαντικά παραμέτρους της συνολικής βαρύτητας της νόσου, μεταξύ των οποίων περιλαμβάνονται οι δερματικές βλάβες, ο κνησμός, παράμετροι της ποιότητας ζωής και συμπτώματα άγχους και κατάθλιψης που παρατηρούνται σε αυτούς τους ασθενείς. Το προφίλ ασφάλειας σε αυτή τη μελέτη ήταν παρόμοιο με αυτό που παρατηρήθηκε στις τρεις προηγούμενες θετικές μελέτες Φάσης 3 του dupilumab στη μέτρια έως σοβαρή ατοπική δερματίτιδα."
Άλλα δευτερεύοντα καταληκτικά σημεία της μελέτης αφορούν παραμέτρους που σχετίζονται με την επίδραση του dupilumab στον επίμονο κνησμό που οφείλεται στη νόσο, παραμέτρους της ποιότητας ζωής και συμπτώματα άγχους και κατάθλιψης. Τα αποτελέσματα για αυτά τα δευτερεύοντα καταληκτικά σημεία τη 16η εβδομάδα ήταν τα εξής:
• Η μέση ποσοστιαία βελτίωση από την έναρξη της μελέτης στην ένταση του αναφερόμενου από τον ασθενή κνησμού, με βάση την αριθμητική κλίμακα NRS (Pruritus Numerical Rating Scale/ αριθμητική κλίμακα μέτρησης κνησμού), ήταν 52% και 54% στους ασθενείς που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, αντίστοιχα, σε σύγκριση με 25% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p μικρότερο από 0,0001).
• Το ποσοστό των ασθενών με βελτίωση τεσσάρων μονάδων ή υψηλότερη από την έναρξη της μελέτης σε παραμέτρους της ποιότητας ζωής του ασθενή με βάση τον Δείκτη DLQI (Dermatology Life Quality Index/Δερματολογικός Δείκτης Ποιότητας Ζωής the Dermatology), ήταν 78% και 88% για τους ασθενείς που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, αντίστοιχα, σε σύγκριση με 44% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p μικρότερο από 0,0001).
• Το ποσοστό των ασθενών με βελτίωση τεσσάρων μονάδων ή υψηλότερη από την έναρξη της μελέτης της βαρύτητας της Ατοπικής Δερματίτιδας (ΑΔ), βάσει της μέτρησης POEM (Patient Oriented Eczema Measure/Μέτρηση Βαρύτητας Εκζέματος με βάση τον Ασθενή), ένα εργαλείο που ποσοτικοποιεί τη νόσο σύμφωνα με την εμπειρία των ασθενών, ήταν 76% και 83% για τους ασθενείς που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, αντίστοιχα, σε σύγκριση με 42% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή (p μικρότερο από 0,0001).
Δεν αναφέρθηκαν νέες ανεπιθύμητες ενέργειες κατά τη μελέτη. Το ποσοστό των ασθενών που ανέφερε κάποια ανεπιθύμητη ενέργεια ήταν παρόμοιο σε όλες τις ομάδες θεραπείας. Η επιπεφυκίτιδα ήταν πιο συχνή στους ασθενείς που έλαβαν dupilumab σε συνδυασμό με τοπικά κορτικοστεροειδή, καθώς αναφέρθηκε από το 16% και το 28% των ασθενών που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, αντίστοιχα, σε σύγκριση με 11% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή. Αντιδράσεις στο σημείο έγχυσης αναφέρθηκαν από το 11% και το 4% των ασθενών που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, αντίστοιχα, σε σύγκριση με 5% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή. Λοιμώξεις του δέρματος αναφέρθηκαν από το 4% και το 2% των ασθενών που έλαβαν dupilumab εβδομαδιαίως ή κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή, αντίστοιχα, σε σύγκριση με 8% για τους ασθενείς που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή.
Συνολικά 325 ασθενείς στην Ευρώπη τυχαιοποιήθηκαν σε τρεις ομάδες θεραπείας στο πλαίσιο της μελέτης διάρκειας 16 εβδομάδων για να λάβουν dupilumab 300 mg εβδομαδιαίως με τοπικά κορτικοστεροειδή, dupilumab 300 mg κάθε δύο εβδομάδες με τοπικά κορτικοστεροειδή ή εικονικό φάρμακο με τοπικά κορτικοστεροειδή.
Σχετικά με το dupilumab
Το dupilumab είναι ένα ανθρώπινο μονοκλωνικό αντίσωμα που έχει σχεδιαστεί για να αναστέλλει την υπερενεργή σηματοδότηση των κυτοκινών IL-4 και IL-13.Επιπροσθέτως της μέτριας έως σοβαρής ατοπικής δερματίτιδας, η Sanofi και η Regeneron μελετούν το dupilumab στο πλαίσιο ενός εκτεταμένου προγράμματος κλινικής ανάπτυξης, όπου συγκαταλέγονται το μη ελεγχόμενο επίμονο άσθμα (φάσης 3), οι ρινικοί πολύποδες (φάσης 3) και η ηωσινοφιλική οισοφαγίτιδα (φάσης 2). Οι δυνητικές αυτές χρήσεις βρίσκονται υπό δοκιμή και η ασφάλεια και αποτελεσματικότητά τους δεν έχουν αξιολογηθεί από καμία ρυθμιστική αρχή. Το Dupilumab αναπτύσσεται από κοινού από τη Regeneron και τη Sanofi στο πλαίσιο μιας συμφωνίας παγκόσμιας συνεργασίας.
Τον Μάρτιο του 2017, ο Οργανισμός Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ ενέκρινε το dupilumab στις ΗΠΑ για τη θεραπεία ενηλίκων με μέτρια έως σοβαρή ατοπική δερματίτιδα των οποίων η νόσος δεν ελέγχεται επαρκώς με συνταγογραφούμενες θεραπείες που εφαρμόζονται τοπικά ή στην περίπτωση που οι συγκεκριμένες θεραπείες δεν ενδείκνυνται. Το dupilumab χορηγείται άπαξ υποδορίως σε μία δόση 300 mg (υποδόρια ένεση) κάθε 2 εβδομάδες μετά από μία αρχική δόση φόρτισης (600 mg). Η Ευρωπαϊκή Επιτροπή αναμένεται να λάβει την οριστική απόφαση για την Αίτηση Άδειας Κυκλοφορίας (MAA) του dupilumab στην Ευρωπαϊκή Ένωση, σε συνέχεια της θετικής γνωμοδότησης από την Επιτροπή Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA) στις 21 Ιουλίου, 2017.
Ειδήσεις υγείας σήμερα
Οικολογικός σχεδιασμός: Νέοι κανόνες για να γίνουν τα βιώσιμα προϊόντα ο κανόνας
Οι γυναίκες ιατροί περιθάλπουν καλύτερα τις γυναίκες ασθενείς [μελέτη]
Πώς σχετίζεται το ασβέστιο στο πρωινό ή στο δείπνο με τον κίνδυνο καρδιαγγειακής νόσου [μελέτη]
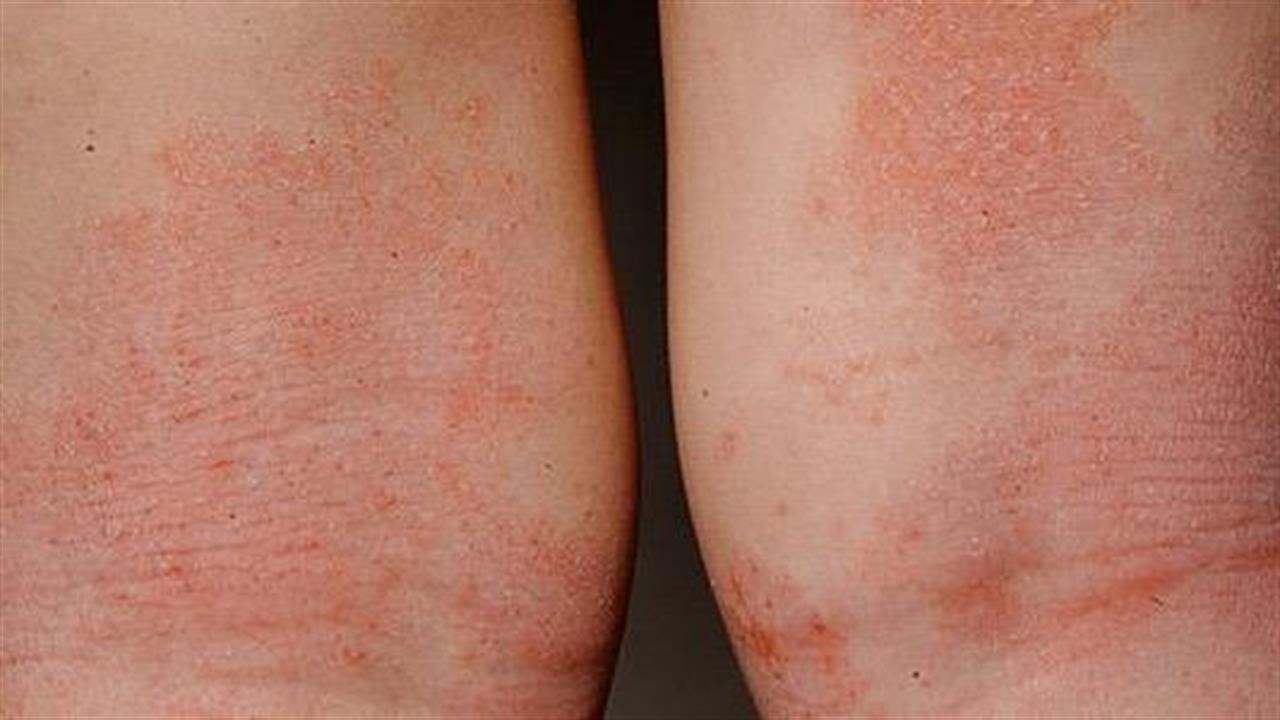
 Ατοπική δερματίτιδα: Από τι άλλο κινδυνεύουν οι μικροί ασθενείς
Ατοπική δερματίτιδα: Από τι άλλο κινδυνεύουν οι μικροί ασθενείς![Η αλλεργία σχετίζεται με σοβαρή πνευμονία από μυκόπλασμα σε παιδιά [μελέτη]](/media/articles/photos/thumb/121289-girldoctor.jpg) Η αλλεργία σχετίζεται με σοβαρή πνευμονία από μυκόπλασμα σε παιδιά [μελέτη]
Η αλλεργία σχετίζεται με σοβαρή πνευμονία από μυκόπλασμα σε παιδιά [μελέτη]  #zisto_alliws: Νέα εκστρατεία ενημέρωσης από τη Pfizer Hellas για την ατοπική δερματίτιδα
#zisto_alliws: Νέα εκστρατεία ενημέρωσης από τη Pfizer Hellas για την ατοπική δερματίτιδα Δράσεις ενημέρωσης και ευαισθητοποίησης για την ατοπική δερματίτιδα
Δράσεις ενημέρωσης και ευαισθητοποίησης για την ατοπική δερματίτιδα Άσπρες κηλίδες στο δέρμα: Οφείλονται στον ήλιο;
Άσπρες κηλίδες στο δέρμα: Οφείλονται στον ήλιο; Η βασική φροντίδα της νευροδερματίτιδας
Η βασική φροντίδα της νευροδερματίτιδας![Οι γυναίκες ιατροί περιθάλπουν καλύτερα τις γυναίκες ασθενείς [μελέτη]](/media/articles/photos/thumb/124428-womandoctorpatient1280.jpg) Οι γυναίκες ιατροί περιθάλπουν καλύτερα τις γυναίκες ασθενείς [μελέτη]
Οι γυναίκες ιατροί περιθάλπουν καλύτερα τις γυναίκες ασθενείς [μελέτη]![Πώς σχετίζεται το ασβέστιο στο πρωινό ή στο δείπνο με τον κίνδυνο καρδιαγγειακής νόσου [μελέτη]](/media/articles/photos/thumb/124441-breakfastcheese1280.jpg) Πώς σχετίζεται το ασβέστιο στο πρωινό ή στο δείπνο με τον κίνδυνο καρδιαγγειακής νόσου [μελέτη]
Πώς σχετίζεται το ασβέστιο στο πρωινό ή στο δείπνο με τον κίνδυνο καρδιαγγειακής νόσου [μελέτη] Nέα προσέγγιση για τον καρκίνο του ήπατος που δεν αντιμετωπίζεται εύκολα
Nέα προσέγγιση για τον καρκίνο του ήπατος που δεν αντιμετωπίζεται εύκολα![Οι γυναίκες αισθάνονται ότι γερνούν πιο αργά από τους άνδρες [μελέτη]](/media/articles/photos/thumb/124421-oldage1280.jpg) Οι γυναίκες αισθάνονται ότι γερνούν πιο αργά από τους άνδρες [μελέτη]
Οι γυναίκες αισθάνονται ότι γερνούν πιο αργά από τους άνδρες [μελέτη] 'Ερχεται το ατομικό clawback στους γιατρούς
'Ερχεται το ατομικό clawback στους γιατρούς Μεχμέτ Χαμεράλ: Ο πρώτος Τούρκος που έγινε μέλος της Ακαδημίας Αθηνών
Μεχμέτ Χαμεράλ: Ο πρώτος Τούρκος που έγινε μέλος της Ακαδημίας Αθηνών Χοληστερίνη: Οι στατίνες, τα μονοκλωνικά αντισώματα και ο στόχος του εμβολίου
Χοληστερίνη: Οι στατίνες, τα μονοκλωνικά αντισώματα και ο στόχος του εμβολίου Πιο θανατηφόρο από πολλές μορφές καρκίνου είναι το κάταγμα στους ηλικιωμένους
Πιο θανατηφόρο από πολλές μορφές καρκίνου είναι το κάταγμα στους ηλικιωμένους "Βρες όσους δεν φαίνονται": Η κρυμμένη καρδιακή ανεπάρκεια
"Βρες όσους δεν φαίνονται": Η κρυμμένη καρδιακή ανεπάρκεια Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους
Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους Διπλή συνδυασμένη μεταμόσχευση ήπατος - νεφρού στο "Ιπποκράτειο" Θεσσαλονίκης
Διπλή συνδυασμένη μεταμόσχευση ήπατος - νεφρού στο "Ιπποκράτειο" Θεσσαλονίκης Πόνος στη δεξιά πλευρά της κοιλιάς: Τι μπορεί να σημαίνει;
Πόνος στη δεξιά πλευρά της κοιλιάς: Τι μπορεί να σημαίνει;