Γράφει ο Δρ Αννίβας Χ. Τσικκίνης (MD-PhD), Χειρουργός - Διευθυντής Ε.Σ.Υ., Χειρουργική Κλινική Μαστού Νοσοκομείο-Μαιευτήριο ‘ΕΛΕΝΑ ΒΕΝΙΖΕΛΟΥ’
Επιδημιολογία
Έχει καταδειχθεί από επιδημιολογικές μελέτες ότι ο καρκίνος του μαστού είναι ο συχνότερος καρκίνος του γυναικείου πληθυσμού στις αναπτυγμένες χώρες του δυτικού κόσμου. Αποτελεί τη δεύτερη αιτία θανάτου από κακόηθες νεόπλασμα και την πρώτη αιτία θανάτου σε γυναίκες ηλικίας 40-49 ετών.
Στην Ελλάδα αντιμετωπίζονται περίπου 4000 νέες περιπτώσεις καρκίνου μαστού κάθε χρόνο. Τα τελευταία 20 χρόνια η συχνότητά του έχει αυξηθεί δραματικά και παρουσιάζεται κυρίως σε γυναίκες 45-55 ετών.
ΚΑΤΑ ΠΡΟΣΕΓΓΙΣΗ Η ΑΠΕΙΚΟΝΙΣΗ ΤΟΥ ΑΡΙΘΜΟΥ ΝΕΩΝ ΠΕΡΙΠΤΩΣΕΩΝ ΚΑΡΚΙΝΟΥ ΤΟΥ ΜΑΣΤΟΥ ΕΤΗΣΙΩΣ
ΠΑΓΚΟΣΜΙΩΣ : 1.200.000
ΗΝΩΜΕΝΕΣ ΠΟΛΙΤΕΙΕΣ : 250.000
ΕΥΡΩΠΗ : 350.000
ΕΛΛΑΔΑ : 4.000
Παράγοντες υψηλού κινδύνου για ανάπτυξη καρκίνου του μαστού και προκαρκινικές καταστάσεις
Η ευρύτατη διάδοση του καρκίνου του μαστού τα τελευταία χρόνια καθιστά αναγκαία την πρόληψη της νόσου, η οποία με τη σειρά της προϋποθέτει τη γνώση των παραγόντων κινδύνου και των καθοριστικών παραγόντων για την ανάπτυξή της.
Φαίνεται ότι η γνώση της γενετικής γύρω από τον καρκίνο μαστού αποτελεί και το κλειδί για τον έλεγχό του, πράγμα που είναι ιδιαίτερα ελπιδοφόρο για τις επόμενες γενεές. Η γνώση των παραγόντων κινδύνου και οι αιτιολογικές υποθέσεις που οδηγούν στην αναγνώρισή τους αποτελούν κατά Boyle την πρωτογενή πρόληψη.
Παράγοντες κινδύνου
Διακρίνονται σε κατηγορίες, ως εξής:
Γενετικοί : φύλο, ηλικία, ύψος, οικογενής και κληρονομικός καρκίνος.
Ορμονικοί : ηλικία, εμμηναρχής και εμμηνόπαυσης, ηλικία κατά τον πρώτο τοκετό, τεκνογονία, θηλασμός, λήψη ορμονών (αντισυλληπτικά, ορμονική θεραπεία υποκατάστασης)
Περιβαλλοντικοί : διαιτητικοί, ιονίζουσα ακτινοβολία, ψυχική ένταση και καρκίνος.
Μορφολογικοί : σχέση κυστικής νόσου και καρκίνος.
Γενετικοί Παράγοντες :
Φύλο : Ο καρκίνος του μαστού είναι 200 φορές συχνότερος στη γυναίκα από τον άνδρα.
Ηλικία : Η συχνότητα εμφάνισης του καρκίνου αυξάνει με την ηλικία και παρουσιάζει ιδιαίτερα ταχείς ρυθμούς αύξησης μεταξύ 40-55 χρόνων. Μετά την εμμηνόπαυση η αύξηση εξακολουθεί, αλλά με βραδύτερο ρυθμό.
Ποσοστό περίπου 50% του συνόλου των καρκίνων του μαστού στις ΗΠΑ αφορά γυναίκες άνω των 65 ετών .
Ύψος : Οι ψηλότερες γυναίκες κινδυνεύουν περισσότερο να προσβληθούν από καρκίνο του μαστού και αυτό γιατί το ύψος συχνά σχετίζεται με το βάρος. Δεν αποκλείεται όμως να υπεισέρχεται και άλλος μηχανισμός, που έχει σχέση με το μέγεθος του μαστού.
(Trichopoulos, de Waard, 1988).
Οικογενειακή προδιάθεση : Οι γυναίκες που έχουν συγγενή πρώτου ή δεύτερου βαθμού προσβεβλημένη από καρκίνο του μαστού παρουσιάζουν αυξημένο κίνδυνο, σύμφωνα με στοιχεία που προκύπτουν από το Κέντρο Ελέγχου της Νόσου και Πρόληψης (CDC), ως εξής :
Προσβεβλημένη μητέρα ή αδελφή - 2,3 σχετικός κίνδυνος
Προσβεβλημένη θεία ή γιαγιά - 1,5 σχετικός κίνδυνος
Προσβεβλημένη μητέρα και αδελφή - 14,0 σχετικός κίνδυνος
Τις τελευταίες δεκαετίες οι γνώσεις μας για τη γενετική αιτιολογία του καρκίνου έχουν αυξηθεί σημαντικά. Πρώτη απόπειρα αναφοράς στη γενετική αιτιολογία του καρκίνου του μαστού έγινε από τον P.
Broca το 1965 ο οποίος περιέγραψε 4 γενεές από την οικογένεια της συζύγου του με καρκίνο του μαστού. Στη μελέτη του συμπεριέλαβε και τον καρκίνο του γαστρεντερικού ως συνδεόμενο με τον κληρονομικό καρκίνο του μαστού (ΚΚΜ).
Σε μερικές οικογένειες ο καρκίνος του μαστού και των ωοθηκών κληρονομούνται. Παρ’ όλα αυτά μόνο ποσοστό 5-10% των καρκίνων των ωοθηκών και του μαστού μπορεί να αποδοθεί στην κληρονομικότητα του καρκινικού γονιδίου.
Το γονίδιο του καρκίνου του μαστού και των ωοθηκών (BRCA1) βρίσκεται στο μακρύ σκέλος του χρωμοσώματος Ι7, οι ερευνητές γενετιστές όμως ανακάλυψαν ύποπτες γενετικές αλλαγές και στο βραχύ σκέλος του 17 χρωματοσώματος, όπου οι μεταλλάξεις της πρωτεΐνης P53, γνωστής ως ογκοκατασταλτικής, προκαλούν γενετική αστάθεια.
Στις ΗΠΑ μία στις 200 γυναίκες είναι κληρονομικά ευπαθής στον καρκίνο του μαστού ο οποίος εμφανίζεται σε νεαρή ηλικία. Οι γυναίκες αυτές απαιτούν έγκαιρη και εντατική παρακολούθηση. Δεν είναι εύκολο να συστήσουμε προφυλακτική μαστεκτομή ή ωοθηκεκτομή επειδή εξάλλου αυτή δεν απομακρύνει τελείως τον κίνδυνο.
Η συχνότητα εμφάνισης καρκίνου του περιτοναίου μετά από ωοθηκεκτομή είναι 2%, ενώ μετά από μαστεκτομή 1%. Χαρακτηριστικά του KKM : κληρονομείται ως αυτόσωμος επικρατής χαρακτήρας, εμφανίζεται σε νεαρή ηλικία και είναι συχνά αμφοτερόπλευρος.
Ορμονικοί παράγοντες :
Ηλικία στον πρώτο τοκετό : Πρόκειται για ένα πολυσυζητημένο θέμα. Η ηλικία κατά τον πρώτο τοκετό φαίνεται να έχει άμεση σχέση με την ανάπτυξη καρκίνου του μαστού. Μία γυναίκα που γέννησε πριν τα 20 έχει 3 φορές μικρότερο κίνδυνο από μία γυναίκα που απέκτησε το πρώτο της παιδί μετά τα 35.
Υπάρχει μία ενδιαφέρουσα άποψη για τη διττή επίδραση της κύησης που διατυπώθηκε από τους M. Lambe, D. Trichopoulos και συν.
Οι συγγραφείς υποστηρίζουν ότι η κύηση αυξάνει τον κίνδυνο αμέσως μετά τον τοκετό, αλλά τον μειώνει μετά παρέλευση ετών. Μια πιθανή βιολογική ερμηνεία είναι ότι τα αυξημένα οιστρογόνα προκαλούν πολλαπλασιασμό των κυττάρων, συμπεριλαμβανομένων όμως και αυτών στα οποία έχει ήδη αρχίσει η κακοήθης εξαλλαγή.
Η μακροχρόνια προστατευτική δράση οφείλεται στις δομικές αλλαγές και τη διαφοροποίηση του μαζικού αδένα, ο οποίος καθίσταται έτσι πιο ανθεκτικός στις καρκινικές διεγέρσεις. Παρόμοια άποψη έχουν διατυπώσει και οι Williams Emi, Jones L., Vessey MP.
Η πολυτοκία συνδυάζεται με αυξημένο κίνδυνο για ανάπτυξη καρκίνου του μαστού σε γυναίκες κάτω των 40 ετών, ενώ σε μεγαλύτερες φαίνεται να παίζει προστατευτικό ρόλο. Στις περιπτώσεις αυτές, πέρα από τη συσσωρευτική επίδραση πολλών κυήσεων είναι πιθανό να επιδρούν προεμμηνοπαυσιακά και άλλοι παράγοντες.
Ο ρόλος των ενδογενών οιστρογόνων αποδεικνύεται από επιδημιολογικά στοιχεία ως εξής :
1. Ο καρκίνος του μαστού είναι 200 φορές πιο συχνός στη γυναίκα παρά τον άνδρα.
2. Εμφανίζεται μετά την ήβη.
3. Ασθενείς με γοναδική αγενεσία, που δεν υποβλήθηκαν σε ορμονική θεραπεία με οιστρογόνα δεν αναπτύσσουν καρκίνο του μαστού.
4. Το 65% των περιπτώσεων συνδυάζεται με καρκίνο του ενδομητρίου.
Η πρώιμη εμμηναρχή και καθυστερημένη εμμηνόπαυση συνιστούν παράγοντες κινδύνου από παλιά αποδεκτούς.
Η προγεννητική έκθεση σε οιστρογόνα φαίνεται να παίζει επίσης κάποιο ρόλο. Μειωμένος κίνδυνος για καρκίνο του μαστού έχει διαπιστωθεί σε γυναίκες που προήλθαν από προεκλαμπτικές μητέρες, γεγονός που πιθανώς οφείλεται στο συνδυασμό της προεκλαμψίας με μειωμένα οιστρογόνα.
Όσο για το ρόλο της προγεστερόνης υπάρχουν αντικρουόμενες απόψεις. Επειδή η μιτωτική δραστηριότητα των μαστικών κυττάρων είναι μεγίστη κατά την εκκριτική φάση του κύκλου, υποστηρίχθηκε ότι η προγεστερόνη προάγει την ανάπτυξη καρκίνου του μαστού.
Μελέτες in vitro όμως των ανθρωπίνων καρκινικών κυττάρων απέδειξαν ότι η προγεστερόνη έχει και διεγερτική αλλά και προστατευτική επίδραση. Καρκινογόνο δράση είναι πιθανό να έχουν και τα ανδρογόνα, αφού η συχνότητα του καρκίνου είναι μεγαλύτερη στην εμμηνόπαυση.
Σε γυναίκες που πρόκειται να αναπτύξουν καρκίνο του μαστού παρατηρούνται από 5 μήνες έως 9 χρόνια νωρίτερα χαμηλά επίπεδα ethiocolanolone που είναι παράγωγο αποβολής ανδροστενδιόνης στα ούρα.
Όσο για τη σχέση του καρκίνου του μαστού με τα αντισυλληπτικά (ΑΣ), η βιβλιογραφία αφθονεί, αλλά δεν αποδεικνύει με πειστικότητα κάποιο αυξημένο κίνδυνο που προκύπτει από αυτά, πράγμα που ισχύει ακόμη και για ασθενείς με οικογενή καρκίνο ή με αποδεδειγμένες καλοήθεις παθήσεις.
Ο θηλασμός, τέλος δεν είναι προστατευτικός, ούτε και η απουσία του είναι επιβαρυντική σε σχέση με τον καρκίνο του μαστού.
Περιβάλλον, δίαιτα. Από τους διαιτητικούς παράγοντες έχει ενοχοποιηθεί περισσότερο η κατανάλωση ζωικού λίπους. Έχει διαπιστωθεί ότι οι Γιαπωνέζες που καταναλώνουν λιγότερο κρέας και λίπος από τις γυναίκες των δυτικών χωρών παρουσιάζουν μειωμένο κίνδυνο για ανάπτυξη καρκίνου του μαστού, πράγμα που δεν ισχύει όμως όταν αυτές μεταναστεύουν σε χώρες με υψηλό κίνδυνο.
Τούτο επισημαίνουν οι συγγραφείς Scaef, Anne Wilson οι οποίοι αποδίδουν με τον όρο ‘κοινωνικός εθισμός’ τη σύγχρονη νοοτροπία για κατανάλωση τυποποιημένων τροφών με αυξημένα λιπαρά.
H παχυσαρκία ευνοεί τη μετατροπή της ανδροστενδιόνης σε οιστρόνη με δυσμενή επίδραση στο μαστό. Ενώ όλα τα λιπαρά σε στερεά μορφή είναι επιβλαβή, το ελαιόλαδο φαίνεται να έχει ευεργετική δράση. Όσο για την κατανάλωση κρέατος υπάρχει μια υπόθεση ότι τα εντερικά βακτήρια στις κρεατοφάγους γυναίκες δια μέσου της β-γλυκουρονιδάσης ευνοούν την απορρόφηση Οιστρογόνων.
Διάγνωση
Η αιτιολογία του καρκίνου του Μαστού είναι άγνωστη, αλλά αρκετοί είναι οι προδιαθεσικοί - επιβαρυντικοί παράγοντες όπως είναι η πρώιμη εμμηναρχή, η καθυστερημένη εμμηνόπαυση, η ατεκνία, η πρώτη εγκυμοσύνη μετά την ηλικία των 35 ετών, το θετικό οικογενειακό ιστορικό και όσον αφορά τον κληρονομικό καρκίνο η εντόπιση γονιδιακών μεταλλάξεων brca 1 και 2.
Στην διάγνωση ενός ψηλαφητού όγκου ακολουθούμε την κλασσική μέθοδο που είναι :
1) Ιστορικό
2) Κλινική εξέταση
3) Μαστογραφία αναλογική ή ψηφιακή, (με ή χωρίς Υπερηχογράφημα και Μαγνητική τομογραφία μαστών)
4 ) Κυτταρολογική εξέταση υλικού μετά από παρακέντηση με λεπτή βελόνη ( FNAC ) ή
5 ) Ιστολογική εξέταση υλικού βιοψίας με κόπτουσα βελόνη (Core biopsy).
Ο συνδυασμός των παραπάνω έχει μεγάλη διαγνωστική ακρίβεια, η οποία στην περίπτωση του ψηλαφητού όγκου φτάνει το 98-99%.
Σε περιπτώσεις αψηλάφητων όγκων που ανευρίσκονται σε προληπτικό έλεγχο με μαστογραφία, για να τεκμηριωθεί η διάγνωση θα χρειασθεί οπωσδήποτε παρακέντηση ή βιοψία, με μαστογραφική ή υπερηχογραφική καθοδήγηση.
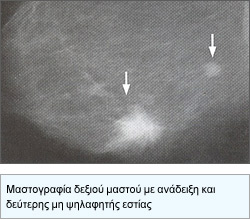
Τα κλασσικά σημεία καρκίνου στην μαστογραφία είναι οι ακτινοειδείς προσεκβολές στην περιφέρεια του όγκου και / ή η παρουσία συρρεουσών, λεπτών ή ποικιλόμορφων αποτιτανώσεων. Είναι βεβαίως πιθανό σε έναν αψηλάφητο καρκίνο στην μαστογραφία, να αναδειχθεί και ένας δεύτερος καρκίνος στον ίδιο ή στον άλλο μαστό.
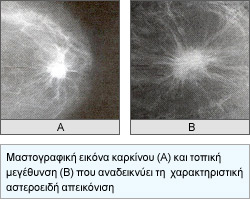
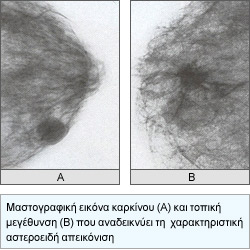
Συμπληρωματικό της μαστογραφίας στη διάγνωση είναι επίσης το Υπερηχογράφημα, το οποίο ελέγχει το περίγραμμα του όγκου (στην περίπτωση καρκίνου είναι ασαφές) και ιδιαίτερα το έγχρωμο υπερηχογράφημα, το οποίο μπορεί να καταδείξει αυξημένη αιμάτωση-αγγείωση της περιοχής στην περίπτωση καρκίνου.
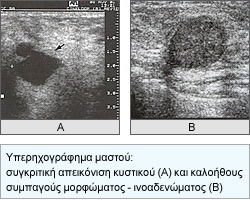
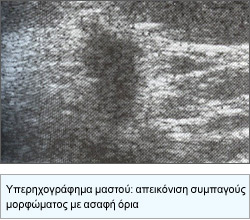
Ακόμα πιο εξειδικευμένη εξέταση είναι και η Μαγνητική μαστογραφία σε ειδικά διαφοροδιαγνωστικά προβλήματα.
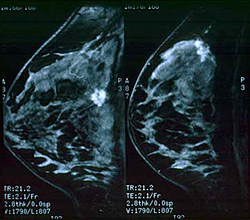
Διαγνωστικές κυτταρολογικές και ιστολογικές τεχνικές
1. Παρακέντηση με λεπτή βελόνη ( FNA ) και Κυτταρολογική εξέταση
Γίνεται σε κάθε ψηλαφητή διόγκωση του μαστού με βελόνη 21 G σε σύριγγα 10 ml και το υλικό που αναρροφάται (υγρό ή κύτταρα) αποστέλλεται για κυτταρολογική εξέταση. Μέθοδος με ευαισθησία που κυμαίνεται από 78-99%. Δυσκολία στην ανίχνευση ορισμένων μορφών καρκίνου όπως λοβιακός, θηλώδης, σωληνώδης, το DCIS κ.αλ.
Σε περιπτώσεις μη ψηλαφητών όγκων είναι δυνατή η παρακέντηση με καθοδήγηση των υπερήχων.
2. Βιοψία με κόπτουσα βελόνη ( Core - biopsy )
Γίνεται συνήθως για λήψη υλικού σε περιπτώσεις τοπικά προχωρημένου καρκίνου του μαστού όπου λαμβάνεται ιστός για ιστολογική επιβεβαίωση, μέτρηση ορμονικών υποδοχέων και ανίχνευση ογκογονιδίων (c-erb-B2, p53, Ki67) ούτως ώστε να μην καθυστερήσει η έναρξη της συστηματικής θεραπείας.
Όπως και παραπάνω σε περιπτώσεις μη ψηλαφητών όγκων που αναδείχθηκαν τυχαία σε μαστογραφία ελέγχου, είναι δυνατή η στερεοτακτική βιοψία με κόπτουσα βελόνη ( Stereotactic core-biopsy) με την καθοδήγηση των υπερήχων ή στερεοτακτικού μηχανήματος προσαρμοσμένου στο μαστογράφο.
Διαδερμικές, στερεοτακτικές τεχνικές διάγνωσης και θεραπευτικής αντιμετώπισης αψηλάφητων αλλοιώσεων
( Minimal invasive diagnostic techniques )
Οι τεχνικές αυτές έχουν αναπτυχθεί τα τελευταία χρόνια για την αντιμετώπιση αψηλάφητων, μαστογραφικών ευρημάτων του μαστού και έχουν σαν στόχο την επαρκή ιστολογική διάγνωση με όσο το δυνατό λιγότερο κόστος και ελάχιστη ταλαιπωρία της ασθενούς, σε συνδυασμό με άριστο αισθητικό αποτέλεσμα.
Επί πλέον στο μέλλον θα έχουν σαν στόχο, την εφαρμογή τους στην αφαίρεση και θεραπευτική αντιμετώπιση μερικών τέτοιων μικρών αλλοιώσεων όπως ένα μικρό ινοαδένωμα, περιορισμένης έκτασης μικροαποτιτανώσεων και καρκίνοι μικρού μεγέθους.
1. Στερεοτακτικός ‘τεμαχισμός’ και αφαίρεση του όγκου ( Stereotactic vacuum assisted breast biopsy – Mammotome - BLES )
Στη μέθοδο αυτή χρησιμοποιείται η κόπτουσα βελόνη η οποία κατευθύνεται στην αψηλάφητη αλλοίωση του μαστού με τη βοήθεια των υπερήχων. Προηγείται τοπική αναισθησία στο σημείο εισόδου της βελόνης, ενώ η ασθενής είναι ξαπλωμένη σε ειδική κλίνη βιοψιών.
Η βελόνη με τον ειδικό μηχανισμό με μαχαιρίδιο, αφαιρεί τμήμα του όγκου το οποίο στη συνέχεια αναρροφάται και συλλέγεται από ειδική συσκευή. Η όλη διαδικασία συνεχίζεται μέχρις ότου όλη η βλάβη να αφαιρεθεί εξ ολοκλήρου, πράγμα που μπορεί να ελεγχθεί και να επιβεβαιωθεί με μαστογραφία σε δεύτερο χρόνο.
Αντενδείξεις ή και δυσκολίες στην εφαρμογή της μεθόδου αποτελούν η θέση της αλλοίωσης (υποθηλαία ή κοντά στο θωρακικό τοίχωμα), το μέγεθος της βλάβης (πολύ μικρός συμπαγής όγκος) ή ο βαθμός αξιοπιστίας σε περίπτωση εκτεταμένων μικροαποτιτανώσεων.
2. Σύστημα ΑΒΒΙ ( Advanced Breast Biopsy Instrumentation)
Στη μέθοδο αυτή, στόχος είναι η πλήρης αφαίρεση της βλάβης. Για το σκοπό αυτό αντί για κόπτουσα βελόνη υπάρχει μία κόπτουσα κυλινδρική κάνουλα εκτομής. Το σύστημα αποτελείται από ειδική κλίνη με προσαρμοσμένο το μηχανισμό κατεύθυνσης του κυλίνδρου εκτομής και δυνατότητα περιστροφής για καλύτερη ρύθμιση της κατεύθυνσης εισόδου στο μαστό.
Το σύστημα συνδέεται με ηλεκτρονικό υπολογιστή, στην οθόνη του οποίου απεικονίζονται σε πραγματικό χρόνο όλες οι φάσεις εκτομής, που λαμβάνονται με την τεχνική του μαστογράφου και ελέγχεται άμεσα η πλήρης αφαίρεση της αλλοίωσης.
Αντενδείξεις ή και δυσκολίες ή περιορισμοί αποτελούν όπως και προηγουμένως, η θέση της αλλοίωσης και το μέγεθος της βλάβης που θα πρέπει να είναι μικρότερο από τη διάμετρο του κυλίνδρου εκτομής. Κύρια επιπλοκή και στις δύο τεχνικές είναι η πρόκληση αιματώματος.
Προβληματισμοί- περιορισμοί
Στη μέθοδο του στερεοτακτικού τεμαχισμού το ακριβές μέγεθος ή η έκταση της αλλοίωσης εκτιμάται έμμεσα με υπερηχογραφικό ή μαστογραφικό υπολογισμό πριν την εφαρμογή της τεχνικής, ενώ τα όρια εκτομής δεν είναι δυνατόν να εκτιμηθούν με ακρίβεια.
Επί πλέον σε περιπτώσεις μικροαποτιτανώσεων περιοχές μικροδιήθησης ή εστίας διηθητικού καρκίνου λίγων χιλιοστών μπορεί να καταστραφούν με τη μέθοδο του τεμαχισμού. Παρόλο που δεν υπάρχουν ενδείξεις για διασπορά της νόσου είναι απαραίτητο να έχουμε αποτελέσματα κλινικών μελετών για αρκετό διάστημα παρακολούθησης.
Στη δεύτερη περίπτωση, υπάρχουν περιορισμοί στην εκτίμηση του μεγέθους αλλά και της σχέσης του μεγέθους με τη διάμετρο του κυλίνδρου εκτομής.
Χειρουργική αντιμετώπιση
Πρώιμος καρκίνος μαστού (στάδια Ι-ΙΙ) θεραπευτικές επιλογές
- Η έκταση της τοπικής θεραπείας της νόσου δεν επηρεάζει την επιβίωση των ασθενών.
- Η συντηρητική χειρουργική αντιμετώπιση του σταδίου Ι - ΙΙ με Ακτινοθεραπεία, επιτυγχάνει παρόμοια αποτελέσματα επιβίωσης και ελέγχου της τοπικής / περιοχικής υποτροπής, με τη ριζική ή τροποποιημένη ριζική μαστεκτομή.
- Ευρεία εκτομή όγκου, χωρίς λεμφαδενικό έλεγχο και ανεπαρκή χορήγηση ακτινοθεραπείας, απολήγει σε βραχύτερη επιβίωση και αυξημένη συχνότητα τοπικών υποτροπών.
- Μαστεκτομή με χαμηλό λεμφαδενικό καθαρισμό και ευρεία εκτομή με λεμφαδενικό έλεγχο και μετεγχειρητική ακτινοθεραπεία, χωρίς σημαντική διαφορά στην επιβίωση ή την τοπική υποτροπή.
- Τροποποιημένη Ριζική Μαστεκτομή και Ογκεκτομή με πλήρη λεμφαδενικό καθαρισμό, με ή χωρίς συμπληρωματική ακτινοθεραπεί , χωρίς διαφορά.
- Συστηματική θεραπεία (χημειοθεραπεία ή χορήγηση ορμονοθεραπείας ή συνδυασμός) μειώνει τη συχνότητα τοπικής υποτροπής.
- Αντένδειξη εφαρμογής συντηρητικών επεμβάσεων.
- Βιολογική συμπεριφορά τοπικής υποτροπής.
Θεραπευτική αντιμετώπιση καρκίνου μαστού
Σήμερα με τα διαγνωστικά μέσα που διαθέτουμε, στη συντριπτική πλειοψηφία των ασθενών έχουμε θέσει προεγχειρητικά τη διάγνωση του καρκίνου. Σε ορισμένες περιπτώσεις ή ακόμη και για λόγους επιβεβαίωσης της διάγνωσης, σε αμφισβητούμενες περιπτώσεις θα χρειασθεί να προηγηθεί ταχεία βιοψία του όγκου.
Η ταχεία βιοψία είναι εξαιρετικά ακριβής μέθοδος για τη διάγνωση ενός διηθητικού καρκίνου.
Παράγοντες που μετρώνται σε μόνιμες τομές και λαμβάνονται υπ΄όψιν στους θεραπευτικούς χειρισμούς είναι η παρουσία οιστρογονικών και προγεστερονικών (ER και PR) υποδοχέων, το Grade του όγκου, η παρουσία νέκρωσης και καρκινικών εμβόλων σε αγγεία και λεμφαγγεία, DNA ανάλυση, ογκογονίδιο c-erb-B2, παρουσία πρωτεϊνών κυτταρικής απόπτωσης p53 και αντιγόνων κυτταρικού πολλαπλασιασμού Ki67.
Η θεραπευτική αντιμετώπιση του καρκίνου του μαστού περιλαμβάνει τέσσερεις χειρισμούς.
- Χειρουργική αντιμετώπιση
- Ακτινοθεραπεία
- Χημειοθεραπεία και
- Ορμονικοί χειρισμοί.
Ανάλογα με την έκταση της χειρουργικής εκτομής, οι επεμβάσεις που μπορεί ο χειρουργός να εκτελέσει διακρίνονται σε Συντηρητικές και Ριζικές.
Συντηρητικές Χειρουργικές Επεμβάσεις
Σαν όρος αναφέρεται στην ευρεία τοπική εκτομή (Wide Local Excision) και στην τεταρτεκτομή (Quadrantectomy), οι οποίες συνδυάζονται με πλήρη ή χαμηλό λεμφαδενικό καθαρισμό. Έχουν κερδίσει πολύ μεγάλο έδαφος τελευταία, διότι διατηρούν το μαστό με καλύτερο αισθητικό αποτέλεσμα και συνδυαζόμενες με ακτινοθεραπεία, επιτυγχάνουν εξίσου καλά αποτελέσματα με τη μαστεκτομή, όσον αφορά και στην τοπική υποτροπή και τη συνολική επιβίωση.
1. Βιοψία ( Excisional biopsy )
Ισοδυναμεί με την ευρεία ογκεκτομή, κατά την οποία αφαιρείται μόνον ο ψηλαφητός όγκος. Μεγάλη σημασία πρέπει να δίνεται στην αφαίρεση επί υγιών ορίων.
2. Ευρεία τοπική εκτομή ( Wide Local Excision )
Είναι η εκτομή του όγκου μαζί με υγιές τμήμα μαστού τουλάχιστον 2 εκ. γύρω από αυτόν. Επέκταση της επέμβασης αυτής είναι η τεταρτεκτομή (quadrantectomy) κατά την οποία αφαιρείται όλο το τεταρτημόριο του μαστού, στο οποίο υπήρχε ο όγκος.
3. Ολική ή Απλή Μαστεκτομή (Total or Simple Mastectomy)
Είναι η αφαίρεση ολόκληρου του μαζικού αδένα μαζί με το δέρμα.
Οι παραπάνω επεμβάσεις αναφέρονται μόνον στο μαστό. Μπορούν όμως να συνοδεύονται από λεμφαδενικό έλεγχο ή δειγματοληψία λεμφαδένων της συστοίχου μασχάλης, χαμηλό ή πλήρη λεμφαδενικό καθαρισμό.
4. Ριζική Μαστεκτομή (Radical Mastectomy)
Διαχωρίζεται στην κλασική Ριζική Μαστεκτομή, την Τροποποιημένη Ριζική Μαστεκτομή και την Εκτεταμένη Ολική Μαστεκτομή.
Α) Η κλασική Ριζική Μαστεκτομή περιγράφηκε για πρώτη φορά από τον Halsted το 1894 όταν ανέλυσε τα αποτελέσματα των χειρουργικών επεμβάσεων για τη θεραπεία του καρκίνου του Μαστού που έγιναν στο Johns Hopkins Hospital από το 1889 έως το 1894 και περιλαμβάνει την εκτομή όλου του μαζικού αδένα μαζί με το περιεχόμενο της συστοίχου μασχάλης και του μείζονος και του ελάσσονος θωρακικού μυός.
Σήμερα εφαρμόζεται σε πολύ σπάνιες περιπτώσεις και δή σε όγκους με εκτεταμένη διήθηση του μείζονος ή/ και του ελάσσονος θωρακικού μυός.
Β) Η Τροποποιημένη Ριζική Μαστεκτομή περιγράφηκε από τον Patey το 1948 και είναι παρόμοια της κλασικής ριζικής μαστεκτομής, με διαφορά τη διατήρηση του μείζονα θωρακικού μυός. Η προσπέλαση της κορυφής της μασχάλης επιτυγχάνεται με τη διατομή του ελάσσονος θωρακικού μυός, κοντά στην πρόσφυσή του στην κορακοειδή απόφυση.
Τροποποίησή της αποτελεί η αφαίρεση του ελάσσονος θωρακικού μυός, με κύριο σκοπό τον καλύτερο καθαρισμό των λεμφαδένων τα μασχάλης καθώς και των λεμφαδένων Rotter.
Γ) Η Εκτεταμένη Ολική Μαστεκτομή είναι η επέμβαση που αντικατέστησε τη ριζική μαστεκτομή τα τελευταία χρόνια. Περιλαμβάνει την ολική αφαίρεση του μαζικού αδένα με το υπερκείμενο δέρμα, το σύμπλεγμα της θηλής με την άλω και πλήρη λεμφαδενικό καθαρισμό της σύστοιχης μασχάλης.
Η προσπέλαση της μασχάλης γίνεται με έλξη και απώθηση χωρίς όμως διατομή ή αφαίρεση του μείζονος και ελάσσονος θωρακικού μυός. Αρχικά παρασκευάζονται οι δερματικοί κρημνοί μέχρι την περιτονία του μείζονος θωρακικού μυός (άνω κρημνός) μέχρι και την παρασκευή του πλαγίου θωρακικού τοιχώματος.
Εν συνεχεία αφαιρείται το περιεχόμενο της μασχάλης αφού παρασκευασθεί και διαφυλαχθεί η μασχαλιαία φλέβα και βεβαίως αφού αναγνωρισθούν και διατηρηθούν το μακρό θωρακικό νεύρο και το θωρακορραχιαίο δεμάτιο.
5. Μαστεκτομή με διατήρηση δέρματος (Skin-sparing Mastectomy)
Στην επέμβαση αυτή αφαιρείται όλο το σύμπλεγμα θηλής-άλω, ο μαζικός αδένας με το περιεχόμενο της μασχάλης με διατήρηση όμως μεγάλου τμήματος του δέρματος. Για να καλυφθεί το έλλειμμα της περιοχής της θηλής με την άλω απαιτείται μόνο ένα μικρό μόσχευμα ενώ η αποκατάσταση γίνεται με μυοδερματικούς κρημνούς ή με πρόθεμα σιλικόνης.
6. Υποδόριος Μαστεκτομή (Subcutaneous Mastectomy)
Στην Υποδόριο Μαστεκτομή το υπερκείμενο δέρμα, αποχωρίζεται από το μαστό και αφαιρείται όσο το δυνατόν περισσότερος μαζικός αδένας ούτως ώστε να φτάσει κανείς στην αφαίρεση ακόμα και του 95 % του αδένα μέχρι και την ουρά του μαστού.
Παραμένει ένα ελάχιστο τμήμα αδενικού ιστού κάτω από τη θηλή, με σκοπό τη διαφύλαξη της αιμάτωσης και αποφυγή τυχόν νέκρωσης της θηλής. Η άμεση αποκατάσταση από την οποία συνοδεύεται, γίνεται συνήθως με τοποθέτηση ενός διατατήρα ιστών (tissue expander) με αντικατάσταση σε δεύτερο χρόνο με μόνιμο πρόθεμα σιλικόνης κι ενδεχομένως με δυνατότητα διάτασης (Becker).
Προσχεδιασμένες (Blichert - Toft et al 1988, Sarrazin et al 1989, Veronezi et al 1990, Fisher et al 1992, Fisher and Anderson 1994) και αναδρομικές μελέτες (Almaric et al 1982, Osborne 1984, Haffty 1989) έχουν ήδη τεκμηριώσει ότι η συντηρητική χειρουργική αντιμετώπιση του πρώιμου καρκίνου του μαστού (στάδια Ι και ΙΙ) συνοδευόμενη από τοπική ακτινοθεραπεία επιτυγχάνει παρόμοια αποτελέσματα επιβίωσης και ελέγχου της τοπικής / περιοχικής υποτροπής με τα αντίστοιχα της ριζικής ή τροποποιημένης ριζικής μαστεκτομής.
Η έκταση των συντηρητικών χειρουργικών επεμβάσεων στην αντιμετώπιση του πρώιμου καρκίνου του μαστού, δεν φαίνεται να επηρεάζει την επιβίωση των αρρώστων, όπως έδειξε η μελέτη ΙΙ του Μιλάνου (Veronesi et al 1990). Στη μελέτη αυτή συγκρίθηκαν τα αποτελέσματα της τεταρτεκτομής και της ογκεκτομής με συνοδό λεμφαδενικό καθαρισμό της μασχάλης και συμπληρωματικής χορήγησης ακτινοβολίας και στις δύο περιπτώσεις.
Αντίθετα το ποσοστό των τοπικών υποτροπών ήταν σημαντικά μικρότερο (5,3%) στην περίπτωση της τεταρτεκτομής, σε σχέση με 13,3% στην περίπτωση της ογκεκτομής.
Λεμφαδένας φρουρός ( Sentinel Node )
Τα τελευταία χρόνια έχει γίνει μεγάλη προσπάθεια να περιορισθεί η έκταση της επέμβασης στη μασχάλη, με την ανεύρεση άλλων μεθόδων ασφαλούς σταδιοποίησης, όπως η βιοψία του ‘λεμφαδένα φρουρού’, ο οποίος εντοπίζεται είτε με τεχνικές απεικόνισης με χρωστική, είτε με ανίχνευση της γ-ακτινοβολίας που εκπέμπει ένα ενεθέν ραδιοφάρμακο που καθηλώνεται εκλεκτικά στον ‘λεμφαδένα φρουρό’ και ανιχνεύεται κατά την διάρκεια της επέμβασης με έναν ειδικό στυλεό ανίχνευσης ακτινοβολίας (γ- detecting probe).
Λεμφαδένας φρουρός ονομάζεται ο πρώτος λεμφαδένας, στον οποίο αποχετεύει η περιοχή του καρκινικού όγκου και ο οποίος πρώτος θα δεχθεί τη μετάσταση καρκινικών κυττάρων του όγκου.
Η χρωστική ή / και το ραδιοκολλοειδές, ενίεται ενδοδερμικά στην περιοχή του πρωτοπαθούς όγκου και στην πορεία του προς τη μασχάλη, σταματά πρώτα στο λεμφαδένα φρουρό. Κατά τη διάρκεια της χειρουργικής επέμβασης αναγνωρίζεται είτε οπτικά, στην περίπτωση της χρωστικής είτε με τη βοήθεια στυλεού ανίχνευσης ακτινοβολίας με ηχητικό και οπτικό σήμα σε ηλεκτρονικό υπολογιστή.
Η ανεύρεση και εξέτασή του, χωρίς να προσδιορίζει τον αριθμό των διηθημένων λεμφαδένων, σε μεγάλο βαθμό καταδεικνύει τη διήθηση ή όχι της μασχάλης σε ποσοστό που αναφέρεται έως και 96%. Με τη μέθοδο αυτή η νοσηρότητα του άνω άκρου, σε γυναίκες που υποβάλλονται σε εγχείρηση για καρκίνο του μαστού μειώνεται σημαντικά, γιατί αποφεύγεται περιττός λεμφαδενικός καθαρισμός σε γυναίκες που δεν έχουν διηθημένους λεμφαδένες.
Ο εντοπισμός του λεμφαδένα φρουρού μπορεί να γίνει είτε με τη μέθοδο της χρωστικής, είτε με τη μέθοδο του ραδιοϊσοτόπου ή με συνδυασμό των δύο.
Ειδήσεις υγείας σήμερα
Nέος κύκλος ανοιχτών συναντήσεων με τις τοπικές κοινωνίες για τα τρία νέα νοσοκομεία ΙΣΝ
Συμμετοχή της Ελληνικής φαρμακοβιομηχανίας στην Ευρωπαϊκή Συμμαχία για τα κρίσιμα Φάρμακα
'Ενωση Ασθενών Ελλάδος: Η Θεσσαλονίκη, γέφυρα στα δικαιώματα των ασθενών
 "ΑνθίΖΩ" με την ΑΚΟΣ στην Κύπρο
"ΑνθίΖΩ" με την ΑΚΟΣ στην Κύπρο Eρχονται και άλλα προγράμματα πρόληψης
Eρχονται και άλλα προγράμματα πρόληψης "Και τώρα...αγωνιζόμαστε" - Από το σοκ της διάγνωσης, στη μάχη με τον καρκίνο
"Και τώρα...αγωνιζόμαστε" - Από το σοκ της διάγνωσης, στη μάχη με τον καρκίνο Τα ακάλυπτα κόστη στον μεταστατικό καρκίνο του μαστού
Τα ακάλυπτα κόστη στον μεταστατικό καρκίνο του μαστού Nέα προσέγγιση για τον καρκίνο του ήπατος που δεν αντιμετωπίζεται εύκολα
Nέα προσέγγιση για τον καρκίνο του ήπατος που δεν αντιμετωπίζεται εύκολα![Ποιοι κινδυνεύουν περισσότερο από καρκίνο παχέος εντέρου [μελέτη]](/media/articles/photos/thumb/124413-tallfat1280.jpg) Ποιοι κινδυνεύουν περισσότερο από καρκίνο παχέος εντέρου [μελέτη]
Ποιοι κινδυνεύουν περισσότερο από καρκίνο παχέος εντέρου [μελέτη] Ηλίας Μόσιαλος: Γιατί θα αποτύχει ο προσωπικός γιατρός - Τα δομικά προβλήματα του ΕΣΥ
Ηλίας Μόσιαλος: Γιατί θα αποτύχει ο προσωπικός γιατρός - Τα δομικά προβλήματα του ΕΣΥ Πώς ο κομμωτής μπορεί να εντοπίσει ασθένειες των μαλλιών και του δέρματος
Πώς ο κομμωτής μπορεί να εντοπίσει ασθένειες των μαλλιών και του δέρματος![Κλιματισμός και νόσος λεγεωνάριων - Τι πρέπει να γνωρίζουμε [εγκύκλιος υπουργείου Υγείας]](/media/articles/photos/thumb/124497-airconditionmaintenance.jpg) Κλιματισμός και νόσος λεγεωνάριων - Τι πρέπει να γνωρίζουμε [εγκύκλιος υπουργείου Υγείας]
Κλιματισμός και νόσος λεγεωνάριων - Τι πρέπει να γνωρίζουμε [εγκύκλιος υπουργείου Υγείας] Πέθανε ο πατέρας του Γιάννη Καλλιάνου - ΕΔΕ στο νοσοκομείο "Αττικόν"
Πέθανε ο πατέρας του Γιάννη Καλλιάνου - ΕΔΕ στο νοσοκομείο "Αττικόν" Μεχμέτ Χαμεράλ: Ο πρώτος Τούρκος που έγινε μέλος της Ακαδημίας Αθηνών
Μεχμέτ Χαμεράλ: Ο πρώτος Τούρκος που έγινε μέλος της Ακαδημίας Αθηνών Διπλή συνδυασμένη μεταμόσχευση ήπατος - νεφρού στο "Ιπποκράτειο" Θεσσαλονίκης
Διπλή συνδυασμένη μεταμόσχευση ήπατος - νεφρού στο "Ιπποκράτειο" Θεσσαλονίκης Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους
Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους 'Ερχεται το ατομικό clawback στους γιατρούς
'Ερχεται το ατομικό clawback στους γιατρούς Πόνος στη δεξιά πλευρά της κοιλιάς: Τι μπορεί να σημαίνει;
Πόνος στη δεξιά πλευρά της κοιλιάς: Τι μπορεί να σημαίνει; Θ. Ψαλτοπούλου: Αύξηση περιστατικών καρκίνου σε νέες ηλικίες, ειδικά στο γαστρεντερικό
Θ. Ψαλτοπούλου: Αύξηση περιστατικών καρκίνου σε νέες ηλικίες, ειδικά στο γαστρεντερικό Μπορεί η μαστίχα Χίου να βοηθήσει με το σύνδρομο ευερέθιστου εντέρου;
Μπορεί η μαστίχα Χίου να βοηθήσει με το σύνδρομο ευερέθιστου εντέρου;![Υπουργείο Υγείας: Ποιες ιατρικές ειδικότητες χορηγούν υαλουρονικό οξύ και botox [εγκύκλιος]](/media/articles/photos/thumb/124342-114448botox231280.jpg) Υπουργείο Υγείας: Ποιες ιατρικές ειδικότητες χορηγούν υαλουρονικό οξύ και botox [εγκύκλιος]
Υπουργείο Υγείας: Ποιες ιατρικές ειδικότητες χορηγούν υαλουρονικό οξύ και botox [εγκύκλιος]