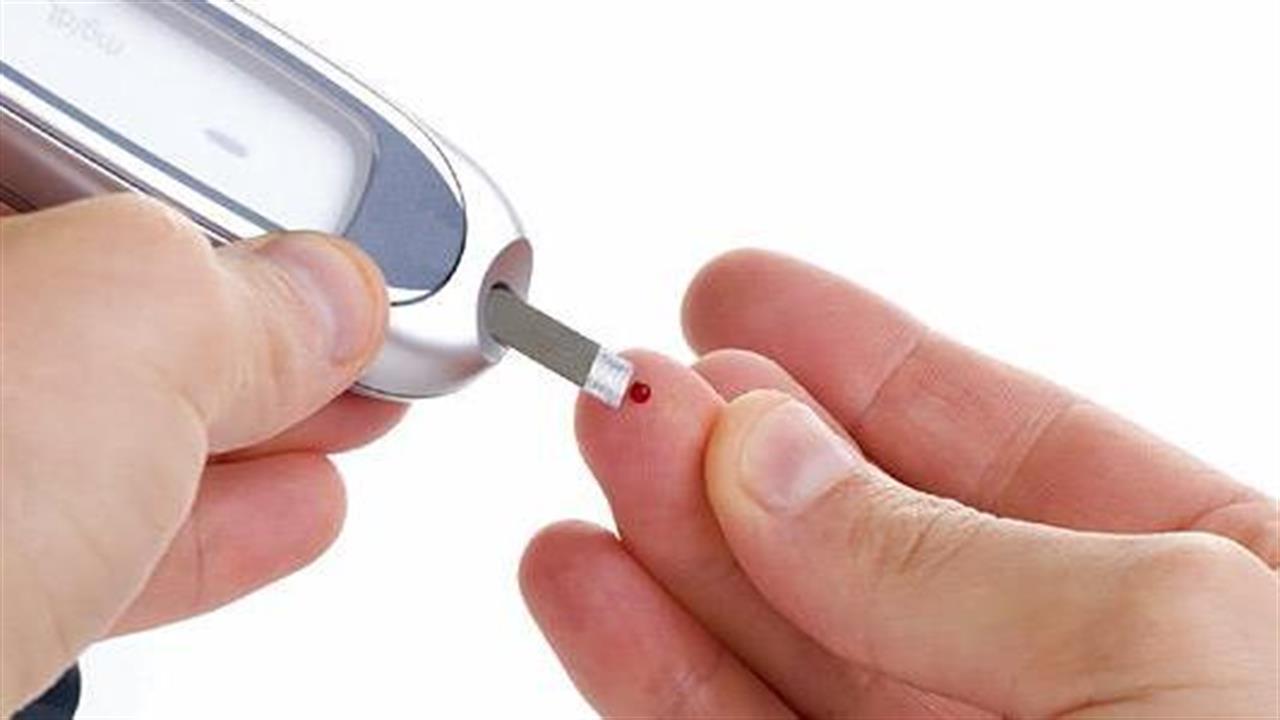
H σεμαγλουτίδη είναι ένα νέο, άπαξ εβδομαδιαίως χορηγούμενο ανάλογο του ανθρώπινου γλυκαγονόμορφου πεπτιδίου 1 (GLP-1), το οποίο έχει ένδειξη είτε ως μονοθεραπεία, όταν η χορήγηση μετφορμίνης αντενδείκνυται, ή δεν είναι εφικτή λόγω μη ανοχής, είτε, ως προσθήκη σε άλλες φαρμακευτικές αγωγές για το σακχαρώδη διαβήτη. Η έγκριση κυκλοφορίας έχει ισχύ σε όλα τα κράτη-μέλη της Ευρωπαικής Ένωσης.
Η Περίληψη Χαρακτηριστικών Προϊόντος αποτυπώνει την ανώτερη και διατηρήσιμη μείωση της HbA1c και του σωματικού βάρους, οι οποίες επιτυγχάνονται με τη σεμαγλουτίδη - σε σχέση με τις άλλες αγωγές με τις οποίες συγκρίθηκε, το καρδιαγγειακό όφελος, καθώς και τη στατιστικά σημαντική μείωση στη διαβητική νεφροπάθεια, η οποία επιτυγχάνεται με τη σεμαγλουτίδη σε σχέση με τη συνήθη αγωγή.
H σεμαγλουτίδη έλαβε έγκριση στην ΕΕ για χρήση σε στιλό πολλαπλών δόσεων, το οποίο ανήκει στις συσκευές χορήγησης τελευταίας γενιάς της Novo Nordisk. Παρόλα αυτά, η Νovo Nordisk σχεδιάζει να αιτηθεί έγκριση από τον Ευρωπαϊκό Οργανισμό Φαρμάκων (ΕΜΑ) και για μια ανανεωμένη έκδοση του στιλό χορήγησης της σεμαγλουτίδης. H διάθεση του νεότερου τύπου στιλό θα διευκολύνει την αποζημίωση της σεμαγλουτίδη σε ασθενείς με σακχαρώδη διαβήτη τύπου 2. Η εμπορική διάθεση της σεμαγλουτίδης αναμένεται να ξεκινήσει στις πρώτες χώρες της ΕΕ το δεύτερο μισό του 2018, ακολουθώντας την έγκριση και της ανανεωμένης έκδοσης του στιλό χορήγησης.
«Είμαστε ιδιαίτερα ενθουσιασμένοι με την έγκριση κυκλοφορίας της σεμαγλουτίδης στην ΕΕ, καθώς πιστεύουμε ότι έχει τη δυναμική να θέσει νέα πρότυπα στη θεραπεία του σακχαρώδους διαβήτη τύπου 2», δήλωσε ο Mads Krogsgaard Thomsen, Executive Vice President και Chief Science Officer της Novo Nordisk. «Ο σακχαρώδης διαβήτης τύπου 2 είναι μια σύνθετη νόσος και το ισχυρό κλινικό προφίλ της σεμαγλουτίδης παρέχει μια αναγκαία θεραπευτική επιλογή για τα άτομα που αναζητούν μια αποτελεσματική λύση για να αντιμετωπίσουν την ασθένειά τους.»
Σεμαγλουτίδη
Η σεμαγλουτίδη είναι ένα νέο, άπαξ εβδομαδιαίως χορηγούμενο, ανάλογο του ανθρώπινου γλυκαγονόμορφου πεπτιδίου 1 (GLP-1), το οποίο αναπτύχθηκε για τη θεραπεία του σακχαρώδους διαβήτη τύπου 2. Η έγκριση της σεμαγλουτίδης βασίστηκε στο πρόγραμμα SUSTAIN, ένα παγκόσμιο πρόγραμμα κλινικής ανάπτυξης το οποίο αποτελείται από οκτώ μελέτες φάσης 3α στο οποίο συμπεριλήφθηκαν περισσότεροι από 8000 ενήλικες με σακχαρώδη διαβήτη τύπου 2. Το κλινικό πρόγραμμα φάσης 3α εξέτασε μεγάλο εύρος προφίλ ατόμων με σακχαρώδη διαβήτη τύπου 2, συμπεριλαμβανομένων τόσο ατόμων με προφίλ υψηλού καρδιαγγειακού κινδύνου, καθώς και ατόμων με και χωρίς νεφρική νόσο. Η σεμαγλουτίδη έλαβε έγκριση κυκλοφορίας στις ΗΠΑ από τον FDA στις 5 Δεκεμβρίου 2017 και στον Καναδά από τον Health Canada στις 9 Ιανουαρίου 2018.
Ειδήσεις υγείας σήμερα
Πρόγραμμα "Προλαμβάνω": Έρχονται προληπτικές εξετάσεις για καρδιά και παχύ έντερο
Εντοπίστηκαν 50 νέες περιοχές του γονιδιώματος που συνδέονται με κίνδυνο εμφάνισης καρκίνου στα νεφρά
Πώς να διαχειριστώ τις σκέψεις ότι η ζωή δεν έχει νόημα
 Εντοπίστηκαν 50 νέες περιοχές του γονιδιώματος που συνδέονται με κίνδυνο εμφάνισης καρκίνου στα νεφρά
Εντοπίστηκαν 50 νέες περιοχές του γονιδιώματος που συνδέονται με κίνδυνο εμφάνισης καρκίνου στα νεφρά Αιμορροφιλία Α: Θετική γνωμοδότηση για θεραπεία από την Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση
Αιμορροφιλία Α: Θετική γνωμοδότηση για θεραπεία από την Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση![Ανεβείτε με τη σκάλα για να ζήσετε περισσότερο [μελέτη]](/media/articles/photos/thumb/124554-stairs.jpg) Ανεβείτε με τη σκάλα για να ζήσετε περισσότερο [μελέτη]
Ανεβείτε με τη σκάλα για να ζήσετε περισσότερο [μελέτη] Η μοναξιά αυξάνει τον κίνδυνο θνητότητας σε επιζώντες από καρκίνο
Η μοναξιά αυξάνει τον κίνδυνο θνητότητας σε επιζώντες από καρκίνο CoViD-19: Συχνότερη η απώλεια όσφρησης μετά από μόλυνση με παραλλαγή Άλφα
CoViD-19: Συχνότερη η απώλεια όσφρησης μετά από μόλυνση με παραλλαγή Άλφα![Ιστορικό καρκίνου αυξάνει τον κίνδυνο καρδιαγγειακών νόσων σε ανθρώπους με υπέρταση [μελέτη]](/media/articles/photos/thumb/124542-121554bloodpressurecheck.jpg) Ιστορικό καρκίνου αυξάνει τον κίνδυνο καρδιαγγειακών νόσων σε ανθρώπους με υπέρταση [μελέτη]
Ιστορικό καρκίνου αυξάνει τον κίνδυνο καρδιαγγειακών νόσων σε ανθρώπους με υπέρταση [μελέτη] Πώς να διαχειριστώ τις σκέψεις ότι η ζωή δεν έχει νόημα
Πώς να διαχειριστώ τις σκέψεις ότι η ζωή δεν έχει νόημα Πρόγραμμα "Προλαμβάνω": Έρχονται προληπτικές εξετάσεις για καρδιά και παχύ έντερο
Πρόγραμμα "Προλαμβάνω": Έρχονται προληπτικές εξετάσεις για καρδιά και παχύ έντερο Μεχμέτ Χαμεράλ: Ο πρώτος Τούρκος που έγινε μέλος της Ακαδημίας Αθηνών
Μεχμέτ Χαμεράλ: Ο πρώτος Τούρκος που έγινε μέλος της Ακαδημίας Αθηνών Μπορεί η μαστίχα Χίου να βοηθήσει με το σύνδρομο ευερέθιστου εντέρου;
Μπορεί η μαστίχα Χίου να βοηθήσει με το σύνδρομο ευερέθιστου εντέρου; Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους
Λευκά αιμοσφαίρια: Τι δείχνουν οι τιμές τους Διπλή συνδυασμένη μεταμόσχευση ήπατος - νεφρού στο "Ιπποκράτειο" Θεσσαλονίκης
Διπλή συνδυασμένη μεταμόσχευση ήπατος - νεφρού στο "Ιπποκράτειο" Θεσσαλονίκης Πόνος στη δεξιά πλευρά της κοιλιάς: Τι μπορεί να σημαίνει;
Πόνος στη δεξιά πλευρά της κοιλιάς: Τι μπορεί να σημαίνει; Θ. Ψαλτοπούλου: Αύξηση περιστατικών καρκίνου σε νέες ηλικίες, ειδικά στο γαστρεντερικό
Θ. Ψαλτοπούλου: Αύξηση περιστατικών καρκίνου σε νέες ηλικίες, ειδικά στο γαστρεντερικό![Στέφανος Κορκολής: Ακόμη έχω καρκίνο, ακόμη το παλεύω [βίντεο]](/media/articles/photos/thumb/124379-stkorkolis241280.jpg) Στέφανος Κορκολής: Ακόμη έχω καρκίνο, ακόμη το παλεύω [βίντεο]
Στέφανος Κορκολής: Ακόμη έχω καρκίνο, ακόμη το παλεύω [βίντεο] Εξόγκωμα πίσω από το αυτί: Τι μπορεί να σημαίνει
Εξόγκωμα πίσω από το αυτί: Τι μπορεί να σημαίνει