Στο 23ο Ετήσιο Συνέδριο της Ευρωπαϊκής Αιματολογικής Εταιρείας (EHA-Ιούνιος 2018) στη Στοκχόλμη ανακοινώθηκαν δεδομένα από το εκτεταμένο πρόγραμμα κλινικών δοκιμών της Celgene για το πολλαπλούν μυέλωμα (ΠΜ). Αυτά τα δεδομένα υποστηρίζουν τη χρήση των ανοσοτροποποιητικών φαρμάκων (IMiDs®) ως θεμελιώδη θεραπεία σε ολόκληρο το θεραπευτικό φάσμα του πολλαπλούν μυελώματος, όταν χορηγούνται είτε ως μονοθεραπεία είτε σε συνδυασμό με άλλες θεραπευτικές κατηγορίες.
Νέα δεδομένα από τη μελέτη OPTIMISMM, μία μελέτη Φάσης III για τη διερεύνηση της αποτελεσματικότητας και της ασφάλειας της πομαλιδομίδης, κατέδειξαν ότι όταν χρησιμοποιήθηκε σε συνδυασμό με βορτεζομίμπη και δεξαμεθαζόνη χαμηλής δόσης, η συνδυασμένη θεραπεία βελτίωσε σημαντικά την επιβίωση χωρίς εξέλιξη της νόσου (PFS) σε σύγκριση με τη βορτεζομίμπη και τη δεξαμεθαζόνη χαμηλής δόσης, σε ασθενείς με υποτροπιάζον και ανθεκτικό πολλαπλούν μυέλωμα που είχαν λάβει στο παρελθόν θεραπεία με λεναλιδομίδη. Η OPTIMISMM είναι η πρώτη προοπτική μελέτη Φάσης III που αξιολόγησε ένα τριπλό θεραπευτικό σχήμα με βάση τα IMiDs® στο πλαίσιο της πρώιμης υποτροπής, στην οποία εντάχθηκαν ασθενείς που είχαν λάβει στο παρελθόν θεραπεία με λεναλιδομίδη και ήταν, στην πλειονότητά τους, ανθεκτικοί σε αυτή.
Στην OPTIMISMM, το συνδυαστικό θεραπευτικό σχήμα της πομαλιδομίδης μείωσε σημαντικά τον κίνδυνο θανάτου ή εξέλιξης της νόσου κατά 39% έναντι της θεραπείας με βορτεζομίμπη και δεξαμεθαζόνη χαμηλής δόσης (11,2 μήνες έναντι 7,1 μηνών, αντίστοιχα, p=<0,0001). Για τους 226 ασθενείς που είχαν λάβει μία προηγούμενη γραμμή θεραπείας, η διάμεση επιβίωση χωρίς εξέλιξη της νόσου ήταν 20,7 μήνες έναντι 11,6 μηνών, αντίστοιχα. Η μελέτη OPTIMISMM μπορεί να αντιπροσωπεύει με μεγαλύτερη ακρίβεια τους ασθενείς με υποτροπιάζον/ανθεκτικό πολλαπλούν μυέλωμα στην καθημερινή κλινική πρακτική σε σύγκριση με άλλες δοκιμές Φάσης III στο υποτροπιάζον/ανθεκτικό πολλαπλούν μυέλωμα, με δεδομένο ότι σχεδόν τα τρία τέταρτα των συμμετεχόντων στη δοκιμή είχαν λάβει προηγουμένως βορτεζομίμπη και όλοι είχαν λάβει λεναλιδομίδη, συμπεριλαμβανομένου ενός ποσοστού 70% που ήταν ανθεκτικοί στη θεραπεία με λεναλιδομίδη.
Περαιτέρω δεδομένα σχετικά με τη χρήση της πομαλιδομίδης στο υποτροπιάζον/ανθεκτικό πολλαπλούν μυέλωμα μετά τη θεραπεία με λεναλιδομίδη προήλθαν από τα αποτελέσματα της ανοιχτής μελέτης Φάσης ΙΙ MM-014 της πομαλιδομίδης σε συνδυασμό με δεξαμεθαζόνη χαμηλής δόσης, με ή χωρίς δαρατουμουμάμπη. Τα ευρήματα που παρουσιάστηκαν στο EHA 2018 κατέδειξαν ότι η θεραπεία με πομαλιδομίδη, δαρατουμουμάμπη και δεξαμεθαζόνη χαμηλής δόσης είχε ως αποτέλεσμα ένα ποσοστό συνολικής ανταπόκρισης (ORR) ίσο με 71,7% σε ασθενείς στη δεύτερη και τρίτη γραμμή θεραπείας, με ποσοστό επιβίωσης στο 1 έτος χωρίς εξέλιξη της νόσου ίσο με 76,9%. Για τους ασθενείς που λάμβαναν θεραπεία τρίτης γραμμής και των οποίων η προηγούμενη θεραπεία με βάση τη λεναλιδομίδη είχε αποτύχει, η θεραπεία με πομαλιδομίδη σε συνδυασμό με δεξαμεθαζόνη χαμηλής δόσης οδήγησε σε ποσοστό συνολικής ανταπόκρισης ίσο με 33,9% και διάμεση επιβίωση χωρίς εξέλιξη της νόσου 12,2 μηνών.
Δεδομένα από δύο επιπρόσθετες αναλύσεις που παρουσιάστηκαν στο EHA 2018 υποδήλωσαν ότι η έγκαιρη και διαρκής αντιμετώπιση ασθενών που πάσχουν από πολλαπλούν μυέλωμα με θεραπείες που βασίζονται σε IMiDs® (λεναλιδομίδη ή πομαλιδομίδη) οδήγησε σε επέκταση του χρόνου έως την επόμενη θεραπεία και σε βελτιωμένη επιβίωση.
Αρχικά, μία αναδρομική μελέτη παρατήρησης έδειξε ότι οι ασθενείς με πολλαπλούν μυέλωμα και κυτταρογενετικές ανωμαλίες υψηλού κινδύνου που έλαβαν θεραπεία συντήρησης με λεναλιδομίδη μετά από μεταμόσχευση αιμοποιητικών κυττάρων είχαν λιγότερες πιθανότητες να προχωρήσουν σε θεραπεία δεύτερης γραμμής σε σύγκριση με εκείνους που δεν έλαβαν θεραπεία συντήρησης με λεναλιδομίδη (24% έναντι 59%, αντίστοιχα). Οι ασθενείς αυτοί είχαν επίσης σημαντικά μεγαλύτερο διάμεσο χρόνο έως την επόμενη θεραπεία (38,8 έναντι 2,8 μηνών, αντίστοιχα, p=<0,001).
Στη δεύτερη ανάλυση, αναπτύχθηκε ένα μοντέλο (CONNECT® MM) που χρησιμοποίησε την προοπτική παρακολούθηση μίας κοόρτης (ομάδα ασθενών που μοιράζονται τα ίδια χαρακτηριστικά) για την εξέταση των κλινικών εκβάσεων με βάση τη θεραπευτική αλληλουχία στο πολλαπλούν μυέλωμα. Τα ευρήματα έδειξαν ότι ο χρόνος επιβίωσης ήταν μεγαλύτερος για τους ασθενείς που έλαβαν για πρώτη φορά θεραπεία με λεναλιδομίδη ή πομαλιδομίδη, με ή χωρίς έναν αναστολέα πρωτεασώματος, και στη συνέχεια άλλαξαν σε θεραπεία με λεναλιδομίδη ή πομαλιδομίδη, σε συνδυασμό με έναν αναστολέα πρωτεασώματος (διάμεση συνολική επιβίωση = 61,9 μήνες, ποσοστό 3ετούς επιβίωσης = 71%). Τα αποτελέσματα υποδηλώνουν ότι η θεραπεία με λεναλιδομίδη ή πομαλιδομίδη κατά το χρονικό σημείο της εξέλιξης της νόσου μπορεί να παρέχει οφέλη που διατηρούνται ακόμη και σε ασθενείς που παρουσίασαν κατά το παρελθόν εξέλιξη με ένα θεραπευτικό σχήμα με βάση τη λεναλιδομίδη ή την πομαλιδομίδη.
Το 2018, ένας εκτιμώμενος αριθμός >40.000 νέων περιστατικών πολλαπλού μυελώματος θα διαγνωσθούν μόνο στην Ευρώπη, αν και τα ποσοστά επίπτωσης παρουσιάζουν διακυμάνσεις σε παγκόσμια κλίμακα. Παρά το ότι η κοινότητα του πολλαπλούν μυελώματος καλωσόρισε την πρόοδο που έχει σημειωθεί στη θεραπεία, η οποία έχει βελτιώσει τα ποσοστά επιβίωσης στο διάστημα των τελευταίων 15 ετών,9 η νόσος παραμένει ανίατη.
Παράλληλα η Celgene και η Acceleron Pharma ανακοίνωσαν στο ASH (American Society of Hematology) 2018 τα αποτελέσματα της μελέτης φάσης 3 BELIEVE για την αξιολόγηση του Luspatercept σε ενήλικους ασθενείς με β-θαλασσαιμία
Φορτίο
Δεδομένα από την πιλοτική μελέτη φάσης 3 κατέδειξαν ότι η θεραπεία με το ερευνητικό φάρμακο luspatercept οδήγησε σε σημαντική μείωση του φορτίου μεταγγίσεων σε σύγκριση με το εικονικό φάρμακο. Υποβολές αιτήσεων στις ρυθμιστικές αρχές σε ΗΠΑ και Ευρώπη προγραμματίζονται μέσα στο πρώτο εξάμηνο του 2019
«Επί του παρόντος, το πρότυπο περίθαλψης (standard of care) που βοηθά τους ασθενείς με β-θαλασσαιμία να διαχειριστούν την αναιμία τους είναι δια βίου μεταγγίσεις ερυθρών αιμοσφαιρίων, οι οποίες όμως με την πάροδο του χρόνου μπορεί να οδηγήσουν σε υπερφόρτωση σιδήρου και απειλητικές για τη ζωή συννοσηρότητες», δήλωσε η Maria Domenica Cappellini, M.D., Καθηγήτρια Ιατρικής, Πανεπιστήμιο του Μιλάνο - Fondazione IRCCS. «Αυτά τα ευρήματα από τη μελέτη BELIEVE είναι συναρπαστικά, καθώς υποδηλώνουν ότι το luspatercept μπορεί να βοηθήσει τους ασθενείς να μειώσουν την εξάρτησή τους από τις μεταγγίσεις ερυθρών αιμοσφαιρίων».
Στη μελέτη BELIEVE επετεύχθη το κύριο καταληκτικό σημείο της ερυθροειδούς ανταπόκρισης, το οποίο ορίστηκε ως μείωση κατά ≥33% στο φορτίο μετάγγισης ερυθρών αιμοσφαιρίων (RBC) (με μείωση ≥ 2 μονάδων RBC) κατά τις εβδομάδες 13-24 σε σύγκριση με το αρχικό διάστημα 12 εβδομάδων πριν από την τυχαιοποίηση. Η μελέτη περιλάμβανε επίσης δευτερεύοντα τελικά σημεία που αξιολόγησαν την επίδραση της θεραπείας στο φορτίο μετάγγισης ερυθρών αιμοσφαιρίων. Η μέση μεταβολή του φορτίου μετάγγισης από την έναρξη της μελέτης στις εβδομάδες 13-24 (με luspatercept έναντι εικονικού φαρμάκου) ήταν -1,35 μονάδες ερυθρών αιμοσφαιρίων.
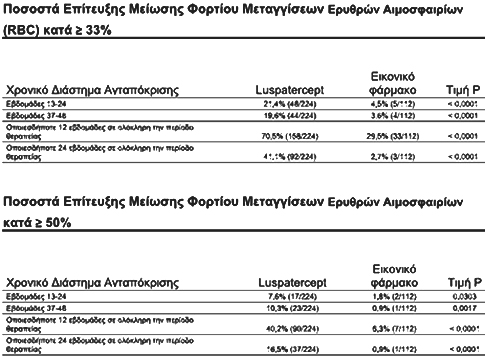
Μεταγγίσεις
«Τα αποτελέσματα της μελέτης BELIEVE καταδεικνύουν τη δυνατότητα του luspatercept να βοηθά τους ενήλικες που ζουν με τη β-θαλασσαιμία να αντιμετωπίζουν καλύτερα την αναιμία τους και να μειώνουν το φορτίο μεταγγίσεων», δήλωσε η Alise Reicin, M.D., President, Global Clinical Development της Celgene. «Αυτά τα αποτελέσματα προάγουν τη γνώση μας σχετικά με το κλινικό προφίλ του luspatercept, η οποία θα συνεχίσει να τροφοδοτεί τα σχέδιά μας για την προώθηση αυτής της πολλά υποσχόμενης ερευνητικής θεραπείας».
Οι εταιρείες προγραμματίζουν τις υποβολές για την έγκριση της άδειας κυκλοφορίας του luspatercept στις ΗΠΑ και την Ευρώπη μέσα στο πρώτο εξάμηνο του 2019.
Το luspatercept είναι ο πρώτος στην κατηγορία του παράγοντας ωρίμανσης ερυθρών (erythroid maturation agent – EMA), ο οποίος πιστεύεται ότι ρυθμίζει την ωρίμανση τελικής φάσης των ερυθρών αιμοσφαιρίων. Η Acceleron και η Celgene αναπτύσσουν από κοινού το luspatercept στο πλαίσιο μίας παγκόσμιας συνεργασίας. Κλινικές μελέτες φάσης 3 συνεχίζουν να αξιολογούν την ασφάλεια και την αποτελεσματικότητα του luspatercept σε ασθενείς με μυελοδυσπλαστικά σύνδρομα (ΜΔΣ) (μελέτη MEDALIST) και σε ασθενείς με β-θαλασσαιμία (μελέτη BELIEVE). Η μελέτη φάσης 3 COMMANDS σε ασθενείς με χαμηλότερου κινδύνου ΜΔΣ που λαμβάνουν θεραπεία πρώτης γραμμής, η μελέτη φάσης 2 BEYOND σε μη μεταγγισιοεξαρτόμενους ασθενείς με β-θαλασσαιμία, καθώς και μία μελέτη φάσης 2 σε ασθενείς με μυελοΐνωση, βρίσκονται σε εξέλιξη.
Πολλαπλό μυέλωμα | βασικά στοιχεία και αριθμοί για τη νόσο
Το πολλαπλό μυέλωμα είναι μια εμμένουσα και απειλητική για τη ζωή μορφή αιματολογικού καρκίνου στην οποία τα πλασματοκύτταρα – σημαντικά στοιχεία του ανοσοποιητικού συστήματος – πολλαπλασιάζονται ανεξέλεγκτα και συσσωρεύονται στον μυελό των οστών.
Παρά το γεγονός πως πρόκειται για μία σπάνια μορφή καρκίνου, το πολλαπλό μυέλωμα είναι ο δεύτερος πιο συχνός αιματολογικός καρκίνος, με περισσότερα από 40.000 νέα περιστατικά ετησίως στην Ευρώπη.
Με την αύξηση που έχει σημειωθεί στο προσδόκιμο ζωής, η επίπτωση του πολλαπλού μυελώματος αναμένεται να αυξηθεί στην Ευρώπη κατά σχεδόν +30% έως το 2040.
Η διάμεση ηλικία κατά τη διάγνωση είναι τα 72 έτη.
Το 25% των ασθενών καταλήγει εντός ενός έτους από τη διάγνωση, ενώ σχεδόν το 40% των ατόμων καταλήγει εντός 5 ετών.
Το ποσοστό επιβίωσης έχει διπλασιαστεί από τις αρχές της δεκαετίας του 2000 με τις νέες καινοτόμες θεραπείες. Παρ' όλα αυτά, το πολλαπλό μυέλωμα παραμένει μια ανίατη νόσος.
β-θαλασσαιμία | βασικά στοιχεία και αριθμοί για τη νόσο
Η β-θαλασσαιμία είναι μία σπάνια, κληρονομική αιματολογική διαταραχή που προκαλείται από ένα γενετικό έλλειμμα της αιμοσφαιρίνης, η οποία εγκαθίσταται στα ερυθρά αιμοσφαίρια (RBC) και μεταφέρει το οξυγόνο σε ολόκληρο τον οργανισμό. Αυτό το έλλειμμα οδηγεί στην παραγωγή μειωμένων και λιγότερο υγιών ερυθρών αιμοσφαιρίων και μπορεί να προκαλέσει βαριάς μορφής αναιμία και άλλα σοβαρά συμπτώματα.
Τύποι
Η β-θαλασσαιμία χωρίζεται συχνά σε δύο κατηγορίες:
· ΜΕΙΖΩΝΑ β-θαλασσαιμία: Τα συμπτώματα εμφανίζονται εντός των πρώτων δύο ετών της ζωής του ατόμου
· ΕΝΔΙΑΜΕΣΗ β-θαλασσαιμία: Εκδηλώνεται συνήθως κατά την προεφηβεία
Επίσης, ορισμένα άτομα μπορεί να φέρουν το γονίδιο της θαλασσαιμίας αλλά να είναι ασυμπτωματικά. Αυτός ο τύπος είναι γνωστός ως ελάσσων.
Πληθυσμός ασθενών
Παγκοσμίως 80-90 εκατομμύρια, το 1,5% του πληθυσμού, είναι ΦΟΡΕΙΣ της γενετικής μετάλλαξης που προκαλεί τη β-θαλασσαιμία.
Η β-θαλασσαιμία εμφανίζεται σε ίδιο ποσοστό στους άνδρες και τις γυναίκες.
Η β-θαλασσαιμία είναι συχνότερη σε χώρες της Μεσογείου, στη Μέση Ανατολή, στην Ινδία και στην Άπω Ανατολή, αλλά ο επιπολασμός της σε παγκόσμια κλίμακα είναι αυξανόμενος.
Στο επικαιροποιημένο Εθνικό Registry για τις αιμοσφαιρινοπάθειες έχουν καταγραφεί 4.032 Έλληνες ασθενείς. (Δημοσίευση Εθνικού Registry, Σεπτέμβριος 2018)
· Οι 2.099 (52,06%) είναι μεταγγισιοεξαρτώμενοι ασθενείς με μείζονα β-θαλασσαιμία και, ενώ οι 873 (21,65%) είναι περιοδικά ή καθόλου μεταγγιζόμενοι.
· Η πλειονότητα των μεταγγισιοεξαρτώμενων ασθενών εντοπίζεται στις ηλικίες 36-45.
· Από τα καταγεγραμμένα θανατηφόρα συμβάντα για την περίοδο 2010-2015, το 28,1% των ασθενών κατέληξε από καρδιακή νόσο και το 23,4% από ηπατική.
· Σε όλο τον κόσμο γεννιούνται κάθε χρόνο περίπου 400.000 παιδιά με αιμοσφαιρινοπάθειες. Στην Ελλάδα, το Εθνικό Κέντρο Θαλασσαιμίας έχει καταφέρει να μειώσει σημαντικά τον αριθμό νεογέννητων με νόσο, μέσα από συντονισμένες προσπάθειες πρόληψης και ενημέρωσης που ξεκίνησαν το 1974. Την περίοδο 2000-2015 καταγράφηκαν μόλις 319 γεννήσεις, ενώ θα αναμένονταν 150-200 γεννήσεις ετησίως, αριθμός που αντιστοιχεί σε περίπου 2.250-3.000 γεννήσεις παιδιών με αιμοσφαιρινοπάθειες για αυτή τη χρονική περίοδο.
Ειδήσεις υγείας σήμερα
Από την έρευνα στην πράξη: Πώς το ΕΔΙΜΟ αλλάζει την ογκολογία στην Ελλάδα
Η Ανοιχτή Αγκαλιά στη Λέρο
Η Πάτρα τίμησε τον Αυξέντιο Καλαγκό
 Η Ανοιχτή Αγκαλιά στη Λέρο
Η Ανοιχτή Αγκαλιά στη Λέρο Η Πάτρα τίμησε τον Αυξέντιο Καλαγκό
Η Πάτρα τίμησε τον Αυξέντιο Καλαγκό Ολοκληρώθηκε η Εβδομάδα Πρόληψης για την Οστεοπόρωση ''Γερά οστά, καλύτερη ζωή!''
Ολοκληρώθηκε η Εβδομάδα Πρόληψης για την Οστεοπόρωση ''Γερά οστά, καλύτερη ζωή!'' Belonging at Work: Όταν η εργασία γίνεται σύμβολο ένταξης και δεύτερων ευκαιριών
Belonging at Work: Όταν η εργασία γίνεται σύμβολο ένταξης και δεύτερων ευκαιριών ‘Ερευνα συνδέει τα στοματικά βακτήρια με τον καρκίνο του στομάχου
‘Ερευνα συνδέει τα στοματικά βακτήρια με τον καρκίνο του στομάχου Καρδιοπάθειες: Πόσο επιβαρύνουν ζέστη, κρύο και ατμοσφαιρική ρύπανση
Καρδιοπάθειες: Πόσο επιβαρύνουν ζέστη, κρύο και ατμοσφαιρική ρύπανση Ουσία του ροδιού μπορεί να προστατεύει από την καρδιοπάθεια [μελέτη]
Ουσία του ροδιού μπορεί να προστατεύει από την καρδιοπάθεια [μελέτη] Ο θόρυβος εξελίσσεται σε σοβαρό κίνδυνο για την υγεία των παιδιών
Ο θόρυβος εξελίσσεται σε σοβαρό κίνδυνο για την υγεία των παιδιών Προσωποποιημένη διατροφή: Το μέλλον στην επιστήμη της διαιτολογίας;
Προσωποποιημένη διατροφή: Το μέλλον στην επιστήμη της διαιτολογίας; Δυστροφική πομφολυγώδης επιδερμόλυση: Επιτυχής η πρώτη χορήγηση γονιδιακής θεραπείας
Δυστροφική πομφολυγώδης επιδερμόλυση: Επιτυχής η πρώτη χορήγηση γονιδιακής θεραπείας Αυξήσεις - φωτιά στο κόστος για kit πρώτων βοηθειών στα αυτοκίνητα
Αυξήσεις - φωτιά στο κόστος για kit πρώτων βοηθειών στα αυτοκίνητα Σύμπραξη ΙΝΕΒ/ΕΚΕΤΑ, AstraZeneca και Γ.Ν. Παπαγεωργίου στην κλινική έρευνα
Σύμπραξη ΙΝΕΒ/ΕΚΕΤΑ, AstraZeneca και Γ.Ν. Παπαγεωργίου στην κλινική έρευνα Πώς θα φροντίσω την υγεία των νεφρών μου
Πώς θα φροντίσω την υγεία των νεφρών μου Τι μπορούμε να κάνουμε για να μειώσουμε την πιθανότητα εμφάνισης άνοιας
Τι μπορούμε να κάνουμε για να μειώσουμε την πιθανότητα εμφάνισης άνοιας Ο πρωινός ύπνος στους ηλικιωμένους ίσως συνδέεται με αυξημένο κίνδυνο θανάτου
Ο πρωινός ύπνος στους ηλικιωμένους ίσως συνδέεται με αυξημένο κίνδυνο θανάτου Η παχυσαρκία ξεκινά από τον εγκέφαλο - Νέα δεδομένα αλλάζουν την κατανόηση της νόσου
Η παχυσαρκία ξεκινά από τον εγκέφαλο - Νέα δεδομένα αλλάζουν την κατανόηση της νόσου Άνοια: Συμπτώματα ανάλογα με το είδος και τη βαρύτητα της νόσου
Άνοια: Συμπτώματα ανάλογα με το είδος και τη βαρύτητα της νόσου