Η Bristol Myers Squibb (BMS) και η Bluebird bio εξασφάλισαν από την Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) προτεραιότητα για την αξιολόγηση της κυτταρικής θεραπείας idecabtagene vicleucel (ide-cel; bb2121) που αφορά το πολλαπλούν μυέλωμα.
Οι εταιρείες ζητούν έγκριση για τη χρήση του ide-cel σε ενήλικες ασθενείς που πάσχουν από τη νόσο και που έχουν υποβληθεί σε τουλάχιστον τρεις προηγούμενες θεραπείες. Η ερευνητική κυτταρική θεραπεία προορίζεται να χρησιμοποιηθεί σε ασθενείς που είχαν υποβληθεί σε θεραπεία με ανοσοδιαμορφωτικό παράγοντα, αναστολέα πρωτεασώματος και αντίσωμα αντι-CD38.
Το FDA πρόκειται να λάβει απόφαση σχετικά με την υποψήφια κυτταρική θεραπεία έως τις 27 Μαρτίου 2021, που είναι η ημερομηνία στόχου του νόμου περί συνταγογράφησης χρηστών φαρμάκων (PDUFA).
Το Ide-cel είναι ανοσοθεραπεία χιμαιρικού αντιγόνου (CAR) που κατευθύνεται από αντιγόνο ωρίμανσης Β-κυττάρων (BCMA), η οποία έχει μια πρωτοποριακή ονομασία θεραπείας (BTD) από τον FDA για υποτροπιάζον και ανθεκτικό πολλαπλό μυέλωμα.
Στην Ευρωπαϊκή Ένωση, ο υποψήφιος για κυτταρική θεραπεία έχει τον χαρακτηρισμό PRIority MEdicines (PRIME) για τις ίδιες ενδείξεις.
Πηγές:
pharmaceutical business review.
Ειδήσεις υγείας σήμερα
Αναβάθμιση Τοπικού Ιατρείου Άνω Λιοσίων σε σύγχρονο Πολυδύναμο Περιφερειακό Κέντρο Υγείας
Ο Ε.Ε.Σ. διοργανώνει διαδικτυακή ημερίδα με θέμα: ''Κλιματική αλλαγή και αστικoί κήποι''
Μείνετε συνδεδεμένοι με τον Όμιλο ΠΡΟΣΥΦΑΠΕ
.jpg)
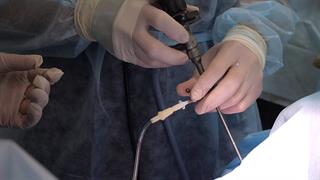 Θρόμβωση: Μπορεί να χρειάζεται προφύλαξη ακόμη και κατά την αρθροσκόπηση γόνατος
Θρόμβωση: Μπορεί να χρειάζεται προφύλαξη ακόμη και κατά την αρθροσκόπηση γόνατος Καρκίνος: Ένεση εξαφάνισε όγκους σε ασθενείς με ανθεκτικό στην αγωγή καρκίνο
Καρκίνος: Ένεση εξαφάνισε όγκους σε ασθενείς με ανθεκτικό στην αγωγή καρκίνο Κολπική μαρμαρυγή: Νέα τεχνολογία υπερτερεί της φαρμακευτικής αγωγής [μελέτη]
Κολπική μαρμαρυγή: Νέα τεχνολογία υπερτερεί της φαρμακευτικής αγωγής [μελέτη]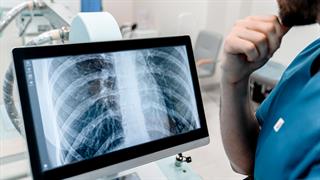 Νέα διαγνωστική μέθοδος απλοποιεί σημαντικά την ανίχνευση της φυματίωσης
Νέα διαγνωστική μέθοδος απλοποιεί σημαντικά την ανίχνευση της φυματίωσης Ημέρα κατά του Καπνίσματος: Οι πολίτες στηρίζουν τις ενιαίες συσκευασίες καπνικών προϊόντων
Ημέρα κατά του Καπνίσματος: Οι πολίτες στηρίζουν τις ενιαίες συσκευασίες καπνικών προϊόντων Εξέταση αίματος εντοπίζει το Alzheimer δεκαετίες πριν [μελέτες]
Εξέταση αίματος εντοπίζει το Alzheimer δεκαετίες πριν [μελέτες] Tσάι: Ποια είναι τα οφέλη της συχνής κατανάλωσης
Tσάι: Ποια είναι τα οφέλη της συχνής κατανάλωσης 373 πνιγμοί κάθε χρόνο στην Ελλάδα - Το 80% αφορούν άτομα άνω των 60 ετών
373 πνιγμοί κάθε χρόνο στην Ελλάδα - Το 80% αφορούν άτομα άνω των 60 ετών Nέες αποχωρήσεις στελεχών
Nέες αποχωρήσεις στελεχών Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου 'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι
'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι Γεωργιάδης - νοσηλευτές: Προκήρυξη 3.694 θέσεων το 2026 και ένταξη στα Βαρέα
Γεωργιάδης - νοσηλευτές: Προκήρυξη 3.694 θέσεων το 2026 και ένταξη στα Βαρέα ΕΟΦ: Προσωρινή απαγόρευση παράλληλων εξαγωγών για 82 φάρμακα [κατάλογος]
ΕΟΦ: Προσωρινή απαγόρευση παράλληλων εξαγωγών για 82 φάρμακα [κατάλογος] Με "Αγάπη" από τη Βασιλική: Παιδοκαρδιολογικό Ιατρείο στο Ιπποκράτειο Θεσσαλονίκης
Με "Αγάπη" από τη Βασιλική: Παιδοκαρδιολογικό Ιατρείο στο Ιπποκράτειο Θεσσαλονίκης Ξεκινώντας από την "κούνια" - Βρέφη, οθόνες και αναπτυξιακά ελλείμματα
Ξεκινώντας από την "κούνια" - Βρέφη, οθόνες και αναπτυξιακά ελλείμματα