Ένα ζευγάρι νέων γονιδιακών θεραπειών υπόσχεται μια πιθανή διαρκή θεραπεία για τη δρεπανοκυτταρική νόσο, αλλάζοντας διακριτικά τις γενετικές πληροφορίες στα κύτταρα του μυελού των οστών των ασθενών, αναφέρουν ερευνητές.
Και οι δύο θεραπείες λειτουργούν ενεργοποιώντας ένα γονίδιο που προάγει την παραγωγή εμβρυϊκής αιμοσφαιρίνης, δήλωσε ο Δρ Lewis Hsu, επικεφαλής του Ιατρικού Συλλόγου στην Ένωση Κυτταρικών Παθήσεων της Αμερικής (Cell Disease Association of America).
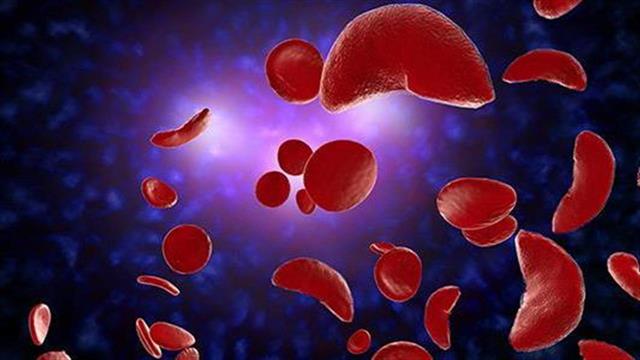
Η δρεπανοκυτταρική νόσος προκαλείται από ένα γενετικό ελάττωμα που οδηγεί τα κανονικά εύκαμπτα ερυθρά αιμοσφαίρια να γίνουν σκληρά και κολλώδη, σχηματίζοντας σχήμα c, σαν δρεπάνι. Αυτά τα ανώμαλα αιμοσφαίρια πεθαίνουν νωρίς, προκαλώντας αναιμία και τείνουν επίσης να πήζουν εύκολα σε μικρά αιμοφόρα αγγεία, προκαλώντας ένα ευρύ φάσμα οδυνηρών και απειλητικών για τη ζωή επιπλοκών.
Και στις δύο νέες θεραπείες, αφαιρούνται δείγματα μυελού των οστών ενός ατόμου και μετά τροποποιούνται γενετικά για να απενεργοποιηθεί το BCL11A , ένα γονίδιο που συνήθως καταστέλλει την παραγωγή εμβρυϊκής αιμοσφαιρίνης.
Τα πρόσφατα επεξεργασμένα βλαστικά κύτταρα του μυελού των οστών τοποθετούνται ξανά στον ασθενή αφού έχουν υποβληθεί σε χημειοθεραπεία για να «καταστραφεί" η ποσότητα των ελαττωματικών κυττάρων μυελού των οστών.
"Πρόκειται για μία παρόμοια διαδικασία με τη μεταμόσχευση μυελού των οστών. Απλώς χρησιμοποιείτε τα δικά σας κύτταρα μυελού των οστών και αυτά τα βλαστικά κύτταρα διορθώνονται, οπότε και τα παίρνετε πίσω", δήλωσε ο Δρ. Banu Aygun, ειδικός στην παιδιατρική αιματολογία-ογκολογία στο Ιατρικό Κέντρο Cohen Children στο New Hyde Park, Νέα Υόρκη.
Η μόνη θεραπεία επι του παρόντος για τη δρεπανοκυτταρική νόσο είναι η μεταμόσχευση μυελού των οστών από έναν υγιή δότη, αλλά αυτή δεν είναι επιλογή για τους περισσότερους ασθενείς, δήλωσε ο Aygun, ο οποίος δεν συμμετείχε στη μελέτη.
Η πρώτη από τις νέες θεραπείες, που αναπτύχθηκε στην Ιατρική Σχολή του Χάρβαρντ από μια ομάδα με επικεφαλής τον Δρ. David Williams, χρησιμοποιεί έναν ιό για να εισαγάγει RNA στον μυελό των οστών που απενεργοποιεί το BCL11A.
Η άλλη μελέτη, αναπτύσσεται από Γερμανούς ερευνητές με επικεφαλής τον Dr. Selim Corbacioglu από το Πανεπιστήμιο του Ρέγκενσμπουργκ, που βασίζεται στην επεξεργασία των γονιδίων CRISPR-Cas9 για να απενεργοποιήσουν το BCL11A.
Η μέθοδος επεξεργασίας γονιδίων CRISPR κέρδισε το Βραβείο Νόμπελ Χημείας 2020 και χρησιμοποιεί χημικές ουσίες για να ανοίξει και να επεξεργαστεί άμεσα τις ακολουθίες DNA, δήλωσε ο Hsu.
Και οι δύο νέες μελέτες γονιδιακής θεραπείας δημοσιεύθηκαν στο Διαδίκτυο, ενώ η γερμανική μελέτη προγραμματίζεται για παρουσίαση το Σάββατο στην εικονική ετήσια συνάντηση της Αμερικανικής Εταιρείας Αιματολογίας.
Τα ευρήματα δείχνουν ότι η δρεπανοκυτταρική νόσος μειώθηκε ή εξαφανίστηκε εντελώς σε έξι ασθενείς που υποβλήθηκαν σε θεραπεία μέσω της μεθόδου Harvard και σε δύο ασθενείς που έλαβαν θεραπεία με τη μέθοδο CRISPR.
Εξαιτίας των παρενεργειών που μπορεί να υπάρχουν (να αποτύχουν,να παράγουν αρκετά αντίγραφα του επεξεργασμένου γονιδίου για να κάνουν τη διαφορά, η γενετική επεξεργασία μπορεί κάπως να αναιρεθεί, ή η επεξεργασία μπορεί να πάει στραβά και, σε χειρότερη περίπτωση, να ενεργοποιήσει γονίδια που προκαλούν καρκίνο) εξήγησε ο Hsu, οι ασθενείς θα πρέπει να παρακολουθούνται τουλάχιστον για δύο χρόνια προκειμένου ο γιατρός να βλέπει την εξέλιξη της θεραπείας και άλλα 15 χρόνια για να αποκλειστεί το ενδεχόμενο εμφάνισης των παρενεργειών.
Πηγές:
New England Journal of Medicine.
Ειδήσεις υγείας σήμερα
Αναβάθμιση Τοπικού Ιατρείου Άνω Λιοσίων σε σύγχρονο Πολυδύναμο Περιφερειακό Κέντρο Υγείας
Ο Ε.Ε.Σ. διοργανώνει διαδικτυακή ημερίδα με θέμα: ''Κλιματική αλλαγή και αστικoί κήποι''
Μείνετε συνδεδεμένοι με τον Όμιλο ΠΡΟΣΥΦΑΠΕ
 Θρόμβωση: Μπορεί να χρειάζεται προφύλαξη ακόμη και κατά την αρθροσκόπηση γόνατος
Θρόμβωση: Μπορεί να χρειάζεται προφύλαξη ακόμη και κατά την αρθροσκόπηση γόνατος Καρκίνος: Ένεση εξαφάνισε όγκους σε ασθενείς με ανθεκτικό στην αγωγή καρκίνο
Καρκίνος: Ένεση εξαφάνισε όγκους σε ασθενείς με ανθεκτικό στην αγωγή καρκίνο Κολπική μαρμαρυγή: Νέα τεχνολογία υπερτερεί της φαρμακευτικής αγωγής [μελέτη]
Κολπική μαρμαρυγή: Νέα τεχνολογία υπερτερεί της φαρμακευτικής αγωγής [μελέτη] Νέα διαγνωστική μέθοδος απλοποιεί σημαντικά την ανίχνευση της φυματίωσης
Νέα διαγνωστική μέθοδος απλοποιεί σημαντικά την ανίχνευση της φυματίωσης Νέα χειρουργική μέθοδος για τον καρκίνο του προστάτη
Νέα χειρουργική μέθοδος για τον καρκίνο του προστάτη Εξέταση αίματος εντοπίζει το Alzheimer δεκαετίες πριν [μελέτες]
Εξέταση αίματος εντοπίζει το Alzheimer δεκαετίες πριν [μελέτες] Tσάι: Ποια είναι τα οφέλη της συχνής κατανάλωσης
Tσάι: Ποια είναι τα οφέλη της συχνής κατανάλωσης 373 πνιγμοί κάθε χρόνο στην Ελλάδα - Το 80% αφορούν άτομα άνω των 60 ετών
373 πνιγμοί κάθε χρόνο στην Ελλάδα - Το 80% αφορούν άτομα άνω των 60 ετών Nέες αποχωρήσεις στελεχών
Nέες αποχωρήσεις στελεχών Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου 'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι
'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι Γεωργιάδης - νοσηλευτές: Προκήρυξη 3.694 θέσεων το 2026 και ένταξη στα Βαρέα
Γεωργιάδης - νοσηλευτές: Προκήρυξη 3.694 θέσεων το 2026 και ένταξη στα Βαρέα ΕΟΦ: Προσωρινή απαγόρευση παράλληλων εξαγωγών για 82 φάρμακα [κατάλογος]
ΕΟΦ: Προσωρινή απαγόρευση παράλληλων εξαγωγών για 82 φάρμακα [κατάλογος] Με "Αγάπη" από τη Βασιλική: Παιδοκαρδιολογικό Ιατρείο στο Ιπποκράτειο Θεσσαλονίκης
Με "Αγάπη" από τη Βασιλική: Παιδοκαρδιολογικό Ιατρείο στο Ιπποκράτειο Θεσσαλονίκης Ξεκινώντας από την "κούνια" - Βρέφη, οθόνες και αναπτυξιακά ελλείμματα
Ξεκινώντας από την "κούνια" - Βρέφη, οθόνες και αναπτυξιακά ελλείμματα