Η εταιρεία Bristol-Myers Squibb ανακοίνωσε ότι ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) επικύρωσε την αίτηση τοποποίησης τύπου ΙΙ, η οποία επιδιώκει να επεκτείνει τις τρέχουσες ενδείξεις για το nivolumab ώστε να συμπεριληφθεί η θεραπεία ασθενών με μελάνωμα οι οποίοι βρίσκονται σε υψηλό κίνδυνο υποτροπής της νόσου μετά από πλήρη χειρουργική εκτομή.
Η επικύρωση της αίτησης επιβεβαιώνει την ολοκλήρωση της υποβολής και ξεκινά την κεντρική διαδικασία εξέτασης της EMA.
"Οι ασθενείς με προχωρημένο μελάνωμα αντιμετωπίζουν συχνά κακή πρόγνωση και έχουν ποσοστό επανεμφάνισης της νόσου του 68% ή και περισσότερο, υπογραμμίζοντας την ανάγκη για πιο αποτελεσματικές θεραπείες του ανοσοενισχυτικού", δήλωσε ο Murdo Gordon, εκτελεστικός αντιπρόεδρος και επικεφαλής εμπορικός διευθυντής στη Bristol-Myers Squibb. "Η επικύρωση της αίτησής μας από τον EMA είναι ένα ακόμη βήμα προς την κατεύθυνση της προσπάθειάς μας να προωθήσουμε τις θεραπείες ανοσο-ογκολογίας για ασθενείς με προχωρημένο μελάνωμα υψηλού κινδύνου στο οποίο έγινε εκτομή’’.
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
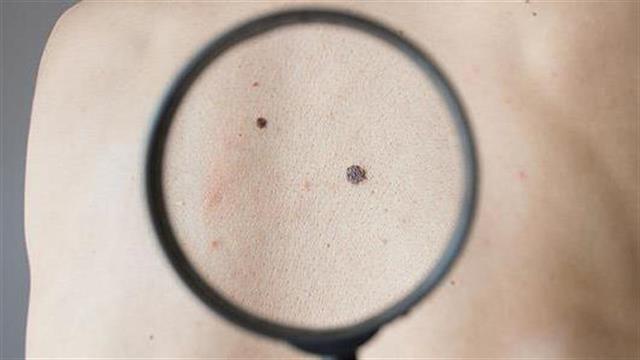
 Μάιος: Μήνας ευαισθητοποίησης για το μελάνωμα - Πρόληψη και θεραπεία
Μάιος: Μήνας ευαισθητοποίησης για το μελάνωμα - Πρόληψη και θεραπεία Μελάνωμα: Συμβουλές για προστασία την άνοιξη
Μελάνωμα: Συμβουλές για προστασία την άνοιξη Μελάνωμα - μελέτη: Μπορεί η δερματοσκόπηση να προβλέψει τον κίνδυνο μετάστασης;
Μελάνωμα - μελέτη: Μπορεί η δερματοσκόπηση να προβλέψει τον κίνδυνο μετάστασης; Η ψωρίαση εμποδίζει την ανάπτυξη καρκίνου του δέρματος
Η ψωρίαση εμποδίζει την ανάπτυξη καρκίνου του δέρματος Μελάνωμα: Σημαντική μείωση της υποτροπής με εμβόλιο mRNA - ανοσοθεραπεία
Μελάνωμα: Σημαντική μείωση της υποτροπής με εμβόλιο mRNA - ανοσοθεραπεία Μελάνωμα: Συνδυαστική θεραπεία μειώνει τον κίνδυνο υποτροπής ή θανάτου
Μελάνωμα: Συνδυαστική θεραπεία μειώνει τον κίνδυνο υποτροπής ή θανάτου Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς