H AbbVie υπέβαλε αιτήσεις που ζητούν έγκριση για τα risankizumab-rzaa, 150 mg και risankizumab, 150 mg στην Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) και στον Ευρωπαϊκό Οργανισμό Φαρμάκων (EMA), αντίστοιχα, για τη θεραπεία ενηλίκων με ενεργή ψωριασική αρθρίτιδα.
Δύο μελέτες Φάσης 3 - KEEPsAKE-1 και KEEPsAKE-2 - υποστήριξαν τις αιτήσεις.
Αυτές οι μελέτες αξιολόγησαν το risankizumab, σε ενήλικες που έπασχαν από ενεργή ψωριασική αρθρίτιδα, συμπεριλαμβανομένων εκείνων που είχαν ανταποκριθεί ανεπαρκώς ή δεν είχαν δυσανεξία στη βιολογική θεραπεία ή / και αντι-ρευματικά φάρμακα που δεν τροποποιούν τη βιολογική νόσο (DMARDs).
Στις μελέτες Φάσης 3 KEEPsAKE-1 και KEEPsAKE-2, το risankizumab, έδειξε αξιοσημείωτες βελτιώσεις στη δραστηριότητα της νόσου, την κάθαρση του δέρματος και τη φυσική λειτουργία την 24η εβδομάδα έναντι του εικονικού φαρμάκου.
Και στις δύο μελέτες, την 24η εβδομάδα έναντι του εικονικού φαρμάκου, σημαντικά περισσότεροι ασθενείς που υποβλήθηκαν σε θεραπεία με risankizumab, πέτυχαν το κύριο τελικό σημείο της απόκρισης ACR20.
Το risankizumab,είναι ένας αναστολέας ιντερλευκίνης-23 (IL-23), ο οποίος αποκλείει επιλεκτικά την IL-23 δεσμεύοντας στην υπομονάδα του p19.
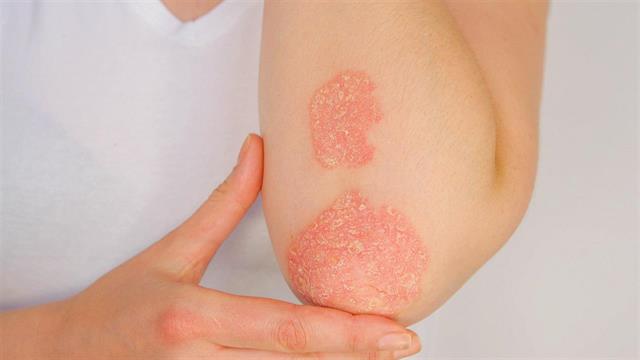
Η ψωριασική αρθρίτιδα είναι μια ετερογενής, συστηματική φλεγμονώδης νόσος με χαρακτηριστικές εκδηλώσεις σε πολλά μέρη του σώματος, συμπεριλαμβανομένων των αρθρώσεων και του δέρματος.
Το risankizumab, αποτελεί μέρος της συνεργασίας μεταξύ AbbVie και Boehringer Ingelheim.
Πηγές:
pharmaceutical-business-review
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
 GLP-1 αγωνιστές: Νέα δεδομένα για πιθανό όφελος στην ψωριασική αρθρίτιδα
GLP-1 αγωνιστές: Νέα δεδομένα για πιθανό όφελος στην ψωριασική αρθρίτιδα Ψωρίαση: Ανακαλύφθηκε η αιτία που ορισμένoι εμφανίζουν ψωριασική αρθρίτιδα
Ψωρίαση: Ανακαλύφθηκε η αιτία που ορισμένoι εμφανίζουν ψωριασική αρθρίτιδα Ψωριασική αρθρίτιδα: Υποσχόμενο φάνηκε φάρμακο σε δοκιμή αρχικού σταδίου
Ψωριασική αρθρίτιδα: Υποσχόμενο φάνηκε φάρμακο σε δοκιμή αρχικού σταδίου Νέα δεδομένα για την ψωριασική αρθρίτιδα και την αξονική σπονδυλαρθρίτιδα
Νέα δεδομένα για την ψωριασική αρθρίτιδα και την αξονική σπονδυλαρθρίτιδα Έρευνα ΡευΜΑζήν & ECONCARE με τη στήριξη της UCB
Έρευνα ΡευΜΑζήν & ECONCARE με τη στήριξη της UCB Μία ακόμη θεραπευτική επιλογή για την ψωρίαση κατά πλάκας και την ενεργό ψωριασική αρθρίτιδα
Μία ακόμη θεραπευτική επιλογή για την ψωρίαση κατά πλάκας και την ενεργό ψωριασική αρθρίτιδα Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς