Τα αποτελέσματα από τη μελέτη Φάσης III ARASENS έδειξαν ότι η χρήση του, από του στόματος, αναστολέα των υποδοχέων ανδρογόνων, της δαρολουταμίδης με αντιανδρογόνα (ADT) και δοσεξατέλη αύξησε σημαντικά τη συνολική επιβίωση (OS) σε ασθενείς με μεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη mHSPC) σε σύγκριση με τον συνδυασμό ADT και δοσεταξέλης. Όπως σημειώνει η Bayer, δαρολουταμίδη συν ADT και δοσεταξέλη μείωσε σημαντικά τον κίνδυνο θανάτου κατά 32,5% σε σύγκριση με τη δοσεταξέλη συν ADT. Κατά την ημερομηνία λήξης συλλογής των δεδομένων για την αρχική ανάλυση (25 Οκτωβρίου 2021), η διάμεση διάρκεια θεραπείας ήταν μεγαλύτερη για τη δαρολουταμίδη συν ADT και δοσεταξέλη (41,0 μήνες) έναντι της ADT συν δοσεταξέλη (16,7 μήνες). Η δαρολουταμίδη συν ADT και δοσεταξέλη έδειξαν επίσης σταθερά οφέλη στα δευτερεύοντα τελικά σημεία και σε προκαθορισμένες υποομάδες. Τα ποσοστά ανεπιθύμητων ενεργειών (ΑΕ) δεν αυξήθηκαν με την προσθήκη δαρολουταμίδης, σημειώνει η εταιρεία. Αυτά τα δεδομένα παρουσιάστηκαν στο ASCO GU Cancers Symposium 2022.και δημοσιεύθηκαν ταυτόχρονα στο έγκριτο επιστημονικό περιοδικό The New England Journal of Medicine.
«Ο μεταστατικός καρκίνος του προστάτη είναι γενικά μία θανατηφόρα ασθένεια και παρά την πρόοδο των τελευταίων ετών, μόνο το 30% αυτών των ανδρών θα επιβιώσει πέραν των πέντε ετών. Η μελέτη ARASENS έδειξε ότι η προσθήκη δαρολουταμίδης, ενός αναστολέα υποδοχέα ανδρογόνων, αύξησε σημαντικά τη συνολική επιβίωση για ασθενείς που έλαβαν την στάνταρντ θεραπεία αντιανδρογόνων και δοσεταξέλης ως αρχική θεραπεία για μεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη. Η δαρολουταμίδη βελτίωσε επίσης τον χρόνο για την εξέλιξη του καρκίνου του προστάτη και άλλα βασικά δευτερεύοντα καταληκτικά σημεία», δήλωσε ο Matthew Smith, MD, Ph.D., Διευθυντής του Προγράμματος για τις Κακοήθειες του Ουροποιογεννητικού, στο Κέντρο Καρκίνου του Γενικού Νοσοκομείου Μασαχουσέτης. «Αυτά τα αποτελέσματα είναι ένα σημαντικό βήμα για το μέλλον στην αντιμετώπιση της νόσου και για τη θεραπεία ασθενών με μεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη».
«Με την προσθήκη των αποτελεσμάτων της μελέτης ARASENS για τους ασθενείς με μεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη στα υπάρχοντα δεδομένα,από τη μελέτη Φάσης ΙΙΙ ARAMIS στον μη μεταστατικό ευνουχοάντοχο καρκίνο του προστάτη, η δαρολουταμίδη έχει πλέον θετικά αποτελέσματα σε δύο βασικές κλινικές δοκιμές για τους ασθενείς σε αυτά τα βασικά στάδια της νόσου», δήλωσε ο Robert LaCaze, Μέλος της Εκτελεστικής Επιτροπής του Τομέα Φαρμάκων της Bayer και Επικεφαλής του Τμήματος Ογκολογίας της Bayer. «Πιστεύουμε ότι η δαρολουταμίδη έχει τη δυνατότητα να γίνει ένα βασικό φάρμακο για κατάλληλους ασθενείς με καρκίνο του προστάτη. Δεσμευόμαστε να καταστήσουμε αυτή την πιθανή νέα θεραπευτική επιλογή στονμεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη διαθέσιμη στους ασθενείς και τους θεράποντες ιατρούς τους και ως εκ τούτου επιταχύνουμε τις διαδικασίες κατάθεσης στις ρυθμιστικές αρχές».
Η μελέτη ARASENS είναι η μόνη τυχαιοποιημένη, προοπτικά σχεδιασμένη, διπλά τυφλή κεντρική μελέτη που συγκρίνει τη χρήση ενός από του στόματος αναστολέα των υποδοχέων ανδρογόνων συν αντιανδρογόνα δεύτερης γενιάς και δοσεταξέλη, με την συνιστώμενη θεραπεία αντιανδρογόνων συν δοσεταξέλης στο μεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη.
Η Bayer σημειώνει ότι η δαρολουταμίδη είναι εγκεκριμένη σε περισσότερες από 60 χώρες σε όλο τον κόσμο, συμπεριλαμβανομένων των ΗΠΑ, της Ευρωπαϊκής Ένωσης (ΕΕ), της Ιαπωνίας και της Κίνας, για τη θεραπεία ασθενών με μη μεταστατικό ευνουχοάντοχο καρκίνο του προστάτη, οι οποίοι διατρέχουν υψηλό κίνδυνο να αναπτύξουν μεταστατική νόσο. Το προϊόν αναπτύσσεται από κοινού από την Bayer και την Orion Corporation, μια φινλανδική φαρμακευτική εταιρεία με παγκόσμια παρουσία. Η ένωση διερευνάται επίσης σε περαιτέρω μελέτες σε διάφορα στάδια του καρκίνου του προστάτη, συμπεριλαμβανομένης μιας άλλης μελέτης Φάσης ΙΙΙ στον μεταστατικό ορμονοευαίσθητο καρκίνο του προστάτη (ARANOTE) καθώς και μιας μελέτης Φάσης ΙΙΙ που πραγματοποιείται υπό την καθοδήγηση της AΝZUPκαι αξιολογεί τη δαρολουταμίδη ως επικουρική θεραπεία για εντοπισμένο καρκίνο του προστάτη με πολύ υψηλό κίνδυνο υποτροπής (DASL-HiCaP, ANZUP1801).
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
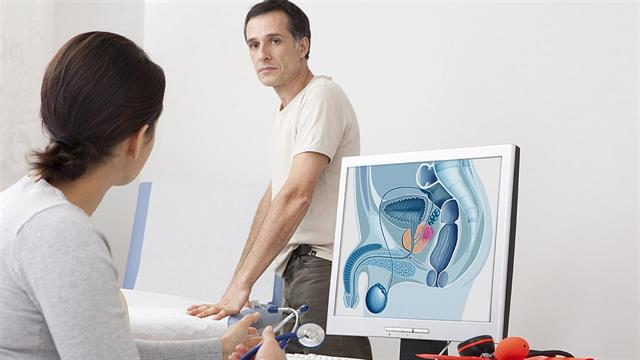
 Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Ozempic και Mounjaro: Ενδείξεις ότι "φρενάρουν" τον καρκίνο
Ozempic και Mounjaro: Ενδείξεις ότι "φρενάρουν" τον καρκίνο Πάνω από 7 δισ. δολάρια η αγορά των τεστ για καρκίνο του τραχήλου - Kυριαρχεί το τεστ Παπ
Πάνω από 7 δισ. δολάρια η αγορά των τεστ για καρκίνο του τραχήλου - Kυριαρχεί το τεστ Παπ Βασιλακόπουλος: Εντυπωσιακά αποτελέσματα στην επόμενη δεκαετία για τα mRNA εμβόλια κατά του καρκίνου
Βασιλακόπουλος: Εντυπωσιακά αποτελέσματα στην επόμενη δεκαετία για τα mRNA εμβόλια κατά του καρκίνου 3ο Συνέδριο Ασθενών: Ο καρκίνος του μαστού στην Ελλάδα σήμερα
3ο Συνέδριο Ασθενών: Ο καρκίνος του μαστού στην Ελλάδα σήμερα Η Agata Jakoncic στο Most Powerful Women Summit 2026
Η Agata Jakoncic στο Most Powerful Women Summit 2026 Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς