Αίσθηση καύσης, φουσκάλες, πόνος: Κάθε χρόνο, περισσότερα από 40 εκατομμύρια άτομα σε όλο τον κόσμο μολύνονται από τον ιό του έρπητα. Για τα νεογέννητα και τα άτομα με εξασθενημένο ανοσοποιητικό σύστημα, ο ιός μπορεί να αποτελεί σοβαρή απειλή. Ερευνητές στο Αμβούργο και στο Γκέτινγκεν κατάφεραν να ανακαλύψουν ένα μίνι αντίσωμα με το οποίο μπορεί να απενεργοποιηθεί μια πρωτεΐνη που είναι απαραίτητη για τη μόλυνση. Τα ευρήματα που δημοσιεύθηκαν στο επιστημονικό περιοδικό "Nature" ανοίγουν μεσοπρόθεσμα νέες δυνατότητες για τη θεραπεία και την πρόληψη σοβαρών λοιμώξεων από έρπητα.
Μόλις μολυνθεί κάποιος, ο ιός του έρπητα παραμένει στον οργανισμό για όλη τη ζωή. Οι πάσχοντες είναι λανθάνων μολυσμένοι. Ο ιός κρύβεται στα νευρικά κύτταρα από το ανοσοποιητικό σύστημα και περιμένει, σε μεγάλο βαθμό ανενεργός, την κατάλληλη στιγμή.
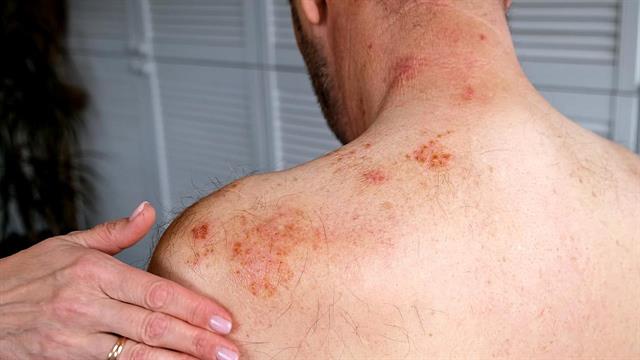
Όταν παρουσιαστεί μια "ευνοϊκή" ευκαιρία – για παράδειγμα, όταν το ανοσοποιητικό σύστημα είναι εξασθενημένο ή σε περίπτωση στρες – ο ιός πολλαπλασιάζεται ξανά, κυρίως για να μολύνει νέους "ξενιστές". Περίπου το 60% του ανθρώπινου πληθυσμού είναι φορέας του ιού του απλού έρπητα τύπου 1 (HSV-1), ο οποίος συνήθως προκαλεί δερματικές αλλοιώσεις και είναι επίσης γνωστός ως έρπης των χειλιών. Σχεδόν το 20% του πληθυσμού πάσχει από έρπητα των γεννητικών οργάνων, ο οποίος προκαλείται κυρίως από τον συγγενή, σεξουαλικά μεταδιδόμενο HSV-2 ή από τον HSV-1.
Αυτό που για τους κατά τα άλλα υγιείς πάσχοντες είναι κυρίως επώδυνο και δυσάρεστο, μπορεί να έχει δραστικές, εν μέρει θανατηφόρες, συνέπειες για άτομα με προϋπάρχουσες παθήσεις. Οι σοβαρές περιπτώσεις επηρεάζουν το κεντρικό νευρικό σύστημα. Ιδιαίτερα ευάλωτα είναι τα νεογνά: εάν η μητέρα έχει ενεργή λοίμωξη από έρπητα, το παιδί μπορεί εύκολα να μολυνθεί κατά τη διάρκεια του τοκετού. Αυτός ο λεγόμενος νεογνικός έρπης συχνά συνοδεύεται από μόνιμες νευρολογικές βλάβες και μπορεί ακόμη και να αποβεί θανατηφόρος για το παιδί.
Για να μολύνει ένα κύτταρο-ξενιστή, ο ιός του έρπητα προσκολλάται πρώτα στην εξωτερική κυτταρική μεμβράνη του. Στο επόμενο στάδιο, συγχωνεύει το μεμβρανικό του περίβλημα με αυτό του κυττάρου-ξενιστή.
Στη συνέχεια, εισάγει το γενετικό του υλικό στο προσβεβλημένο κύτταρο για να παράγει νέους ιούς. Η γλυκοπρωτεΐνη Β (gB) παίζει καθοριστικό ρόλο στη συγχώνευση. Είναι "γεμάτη ενέργεια" και χρησιμοποιεί αυτή την ενέργεια για να συγχωνεύσει το κέλυφος του ιού με την κυτταρική μεμβράνη.
Κατά τη διάρκεια αυτής της διαδικασίας συγχώνευσης, η gB αλλάζει την τρισδιάστατη μορφή της. Αυτό την καθιστά ελκυστικό στόχο για φάρμακα, αλλά μέχρι στιγμής δεν υπάρχουν αντιιικά φάρμακα που να στοχεύουν την gB, καθώς κρίσιμες περιοχές της πρωτεΐνης είναι απρόσιτες ή προστατευμένες.
Ερευνητές του Ινστιτούτου Ιολογίας Leibniz (LIV), του Πανεπιστημίου του Αμβούργου (UHH), και του Πανεπιστημιακού Νοσοκομείου Αμβούργου-Eppendorf (UKE) στο Κέντρο Δομικής Συστημικής Βιολογίας (CSSB) στο Αμβούργο, καθώς και του Ινστιτούτου Max Planck (MPI) για τις Πολυεπιστημονικές Φυσικές Επιστήμες στο Γκέτινγκεν, κατάφεραν να σταθεροποιήσουν τον σύμπλεγμα gB στη μορφή του που ήταν μέχρι τώρα απρόσιτη και έτοιμη για σύντηξη.
Μπόρεσαν να προσδιορίσουν τη δομή του σε υψηλή ανάλυση με τη χρήση κρυο-ηλεκτρονικής μικροσκοπίας, ανάλυσης εικόνας και μοντελοποίησης δομής. Οι τεχνολογικές πλατφόρμες για προηγμένη οπτική μικροσκοπία και κρυο-ηλεκτρονική μικροσκοπία (Kryo-EM) στο CSSB ήταν ουσιαστικής σημασίας για την επιτυχία της έρευνας.
Το νανοσώμα αλπακά εξουδετερώνει την πρωτεΐνη σύντηξης
Η ομάδα του Γκέτινγκεν απομόνωσε από εμβολιασμένα αλπακά ένα μίνι αντίσωμα, ένα λεγόμενο νανοσωματίδιο, το οποίο εξουδετερώνει το gB σε πολύ χαμηλές συγκεντρώσεις. Το νανοσωματίδιο δεσμεύει τη μορφή του gB που είναι έτοιμη για σύντηξη και το εμποδίζει να εκτελέσει τις κινήσεις και να απελευθερώσει την ενέργεια που απαιτείται για τη σύντηξη.
Τα αλπάκα, τα λάμα και άλλα καμήλα έχουν αντισώματα που είναι απλούστερα από τα κανονικά αντισώματα των θηλαστικών. Αυτά μπορούν να μειωθούν περαιτέρω σε εργαστήριο σε λεγόμενα νανοσωματίδια.
Ερευνητές της ομάδας του Kay Grünewald, επικεφαλής του Τμήματος Δομικής Κυτταρικής Βιολογίας των Ιών στο LIV, UHH και CSSB στο Αμβούργο, παρήγαγαν ένα παρασκεύασμα gB, με το οποίο η ομάδα στο Γκέτινγκεν ανοσοποίησε ένα αλπάκα και προκάλεσε την παραγωγή αντισωμάτων. «Η επιβάρυνση για το αλπακά μας, τον Μαξ, ήταν πολύ μικρή, συγκρίσιμη με έναν εμβολιασμό και μια εξέταση αίματος σε ανθρώπους", εξηγεί ο Ντίρκ Γκέρλιχ, διευθυντής στο MPI και επικεφαλής του Τμήματος Κυτταρικής Λογιστικής.
Μετά από μια αιμοδοσία, η αποστολή του Μαξ είχε τελειώσει. Η περαιτέρω εργασία πραγματοποιήθηκε στο εργαστήριο με τη βοήθεια συσκευών υψηλής τεχνολογίας, ενζύμων, βακτηρίων, βακτηριοφάγων και υπολογιστών. Τελικά, τα νανοσώματα παράγονται μικροβιολογικά – δηλαδή με τρόπο παρόμοιο με την μπύρα.
Από το δείγμα αίματος, οι ερευνητές απέκτησαν αρχικά τα σχέδια για περίπου ένα δισεκατομμύριο διαφορετικά νανοσώματα. Ωστόσο, μόνο ένα ελάχιστο ποσοστό από αυτά στοχεύει στον πραγματικό στόχο.
Οι ερευνητές του Γκέτινγκεν απομόνωσαν τα gB-ειδικά νανοσωματίδια με τη βοήθεια βακτηριοφάγων και στη συνέχεια παρήγαγαν μεμονωμένα αντιπροσωπευτικά δείγματα με μικροβιολογικές μεθόδους. Αυτά στη συνέχεια δοκιμάστηκαν στο Αμβούργο για την αντιική τους δράση. "Μπορέσαμε να προσδιορίσουμε με ακρίβεια ένα νανοσωματίδιο που έχει ισχυρή εξουδετερωτική δράση. Το ενδιαφέρον είναι ότι δρα τόσο κατά του HSV-1 όσο και κατά του HSV-2", αναφέρει ο Görlich.
Στο Αμβούργο, η ομάδα κατάφερε να διασαφηνίσει τη δομή 3D του φυσικού HSV-2 gB με το συνδεδεμένο νανοσωματίδιο. Αυτό το μοντέλο και άλλα μοντέλα κρυο-ηλεκτρονικής μικροσκοπίας υψηλής ανάλυσης του gB πριν και μετά τη σύντηξη – που δημιουργήθηκαν με τη βοήθεια της ομάδας της Maya Topf, επικεφαλής του Τμήματος Ολοκληρωμένης Ιολογίας στο LIV, UKE και CSSB, η οποία χρησιμοποίησε προηγμένα υπολογιστικά εργαλεία για τη μοντελοποίηση και την επικύρωση – παρείχαν πληροφορίες για κρίσιμες θέσεις στο gB και αποκρυπτογράφησαν έτσι τον μηχανισμό εξουδετέρωσης. "Τα αποτελέσματά μας υποδηλώνουν ότι η σύνδεση του νανοσωματιδίου εμποδίζει την πρωτεΐνη να αλλάξει τη μορφή της, ώστε να μπορεί να συγχωνεύσει τις μεμβράνες. Έτσι αποτρέπεται η μόλυνση", λέει ο Grünewald.
Οι ανακαλύψεις των ομάδων υπόσχονται μια νέα προσέγγιση για τη θεραπεία και την πρόληψη των λοιμώξεων από έρπητα. «Τα νανοσωματίδια δεν μπορούν να χρησιμοποιηθούν μόνο ως συμπλήρωμα των συνήθων φαρμάκων σε περίπτωση υπάρχουσας λοίμωξης από έρπητα.
Στο μέλλον, θα μπορούσαν να προστατεύσουν άτομα που διατρέχουν ιδιαίτερο κίνδυνο από λοίμωξη από έρπητα ή από την επανεμφάνιση μιας λανθάνουσας λοίμωξης", λέει ο Benjamin Vollmer, επικεφαλής επιστήμονας του έργου στην ομάδα του Grünewald και πρώτος συγγραφέας της μελέτης.
"Μέχρι εκεί είναι ακόμα μακρύς ο δρόμος, αλλά τα άτομα με ιδιαίτερα αδύναμο ανοσοποιητικό σύστημα θα επωφεληθούν ακόμη περισσότερο από τα καινοτόμα αντισώματα. Σε αυτά περιλαμβάνονται, για παράδειγμα, τα νεογέννητα, τα άτομα με HIV και τα άτομα με καρκίνο, αυτοάνοσες ασθένειες ή επικείμενη μεταμόσχευση οργάνου".
Εάν μια έγκυος πάσχει από ενεργή λοίμωξη από έρπητα, η προφυλακτική χορήγηση νανοσωμάτων στη μέλλουσα μητέρα θα μπορούσε να αποτρέψει τη μόλυνση του νεογέννητου. Η αίτηση για δίπλωμα ευρεσιτεχνίας, προκειμένου να αναπτυχθούν περαιτέρω τα νανοσωματίδια για κλινική χρήση και να προσελκυστούν συνεργάτες από τη βιομηχανία, έχει ήδη υποβληθεί.
Πηγές:
Μαx Planck Institut
Ειδήσεις υγείας σήμερα
Eurostat: Χωρίς παιδιά 3 στις 4 ελληνικές οικογένειες [γράφημα, infographic]
Ε.Ε.Σ.: Εκστρατεία ενημέρωσης και πρόληψης για τον Καρκίνο του Μαστού σε Σέρρες, Έδεσσα και Δράμα
Γαλλία: Σε καραντίνα 1.700 άτομα σε κρουαζιερόπλοιο έπειτα από θάνατο συνεπιβάτη τους
 Το περιβάλλον επιβαρύνει την καρδιά: Τι γίνεται με θόρυβο, αιωρούμενα σωματίδια, ζέστη, ρύπους
Το περιβάλλον επιβαρύνει την καρδιά: Τι γίνεται με θόρυβο, αιωρούμενα σωματίδια, ζέστη, ρύπους Δ. Σαρηγιάννης: Τρεις φορές πάνω οι καρκινογόνες ενώσεις στα αιωρούμενα σωματίδια του καπνού στην Πάτρα
Δ. Σαρηγιάννης: Τρεις φορές πάνω οι καρκινογόνες ενώσεις στα αιωρούμενα σωματίδια του καπνού στην Πάτρα Πόσοι υποφέρουν από άσθμα λόγω της μακροχρόνιας έκθεσης στα αιωρούμενα σωματίδια
Πόσοι υποφέρουν από άσθμα λόγω της μακροχρόνιας έκθεσης στα αιωρούμενα σωματίδια  Η ρύπανση από αιωρούμενα σωματίδια προκαλεί φλεγμονές και ασθένειες
Η ρύπανση από αιωρούμενα σωματίδια προκαλεί φλεγμονές και ασθένειες Ερπητοϊοί: Ποιοι έχουν σοβαρότερες επιπτώσεις
Ερπητοϊοί: Ποιοι έχουν σοβαρότερες επιπτώσεις ‘Ερπης ζωστήρας και γνωστική εξασθένηση [μελέτη]
‘Ερπης ζωστήρας και γνωστική εξασθένηση [μελέτη] Eurostat: Χωρίς παιδιά 3 στις 4 ελληνικές οικογένειες [γράφημα, infographic]
Eurostat: Χωρίς παιδιά 3 στις 4 ελληνικές οικογένειες [γράφημα, infographic] Μείωση οιστρογόνων: Φλεγμονή στο ήπαρ και αλλαγές στη χοληστερόλη αυξάνουν τον καρδιακό κίνδυνο
Μείωση οιστρογόνων: Φλεγμονή στο ήπαρ και αλλαγές στη χοληστερόλη αυξάνουν τον καρδιακό κίνδυνο Γαλλία: Σε καραντίνα 1.700 άτομα σε κρουαζιερόπλοιο έπειτα από θάνατο συνεπιβάτη τους
Γαλλία: Σε καραντίνα 1.700 άτομα σε κρουαζιερόπλοιο έπειτα από θάνατο συνεπιβάτη τους Ποιο μοντέλο τεχνητής νοημοσύνης ξεπερνά σημαντικά τον Δείκτη Μάζας Σώματος
Ποιο μοντέλο τεχνητής νοημοσύνης ξεπερνά σημαντικά τον Δείκτη Μάζας Σώματος Βγήκε από τη ΜΕΘ ο Γ. Μυλωνάκης - Το ανακοινωθέν από το νοσοκομείο "Ευαγγελισμός"
Βγήκε από τη ΜΕΘ ο Γ. Μυλωνάκης - Το ανακοινωθέν από το νοσοκομείο "Ευαγγελισμός" Οι δύσκολες ιατρικές αποφάσεις στο τέλος της ζωής - Παίζει ρόλο η ηλικία του ασθενή;
Οι δύσκολες ιατρικές αποφάσεις στο τέλος της ζωής - Παίζει ρόλο η ηλικία του ασθενή; Γεωργιάδης - πόθεν έσχες: 14 ακίνητα - δάνεια 482.858 ευρώ
Γεωργιάδης - πόθεν έσχες: 14 ακίνητα - δάνεια 482.858 ευρώ Καθηγητής Τσακρής: Πόσο επικίνδυνος είναι ο χανταϊός
Καθηγητής Τσακρής: Πόσο επικίνδυνος είναι ο χανταϊός 75% της φαρμακευτικής δαπάνης σε πολυεθνικές - H παραδοχή που άναψε φωτιές
75% της φαρμακευτικής δαπάνης σε πολυεθνικές - H παραδοχή που άναψε φωτιές Προκήρυξη 1.131 θέσεων ειδικευμένων ιατρών ΕΣΥ επί θητεία σε δημόσιες δομές
Προκήρυξη 1.131 θέσεων ειδικευμένων ιατρών ΕΣΥ επί θητεία σε δημόσιες δομές ΙΝΕΠΥ: Διεπιστημονικός διάλογος στο 8ο Πανελλήνιο Συνέδριο Νοσηλευτικών Ερευνών
ΙΝΕΠΥ: Διεπιστημονικός διάλογος στο 8ο Πανελλήνιο Συνέδριο Νοσηλευτικών Ερευνών Νοσοκομείο Καβάλας: Το θερμό επεισόδιο του διοικητή με δύο γιατρούς και οι συλλήψεις
Νοσοκομείο Καβάλας: Το θερμό επεισόδιο του διοικητή με δύο γιατρούς και οι συλλήψεις