Η Janssen-Cilag International NV ανακοίνωσε σήμερα ότι η Επιτροπή Φαρμακευτικών Προϊόντων για Ανθρώπινη Χρήση (CHMP) του Ευρωπαϊκού Οργανισμού Φαρμάκων (EMA) εξέδωσε θετική γνωμοδότηση, η οποία συνιστά την έγκριση της οξικής αμπιρατερόνης στο πλαίσιο ταχείας διαδικασίας αξιολόγησης.
Είναι ένας νέος, αναστολέας βιοσύνθεσης ανδρογόνων για την αντιμετώπιση του καρκίνου του προστάτη που χορηγείται από το στόμα, μια φορά την ημέρα. Η προτεινόμενη ένδειξη είναι η θεραπεία – σε συνδυασμό με πρεδνιζόνη ή πρεδνιζολόνη –του μεταστατικού ανθεκτικού στον ευνουχισμό καρκίνο του προστάτη σε ενήλικες άνδρες των οποίων η νόσος έχει εξελιχθεί κατά τη διάρκεια ή μετά από θεραπεία με χημειοθεραπευτικό σχήμα που περιέχει δοσεταξέλη.
Η CHMP είναι η αρμόδια επιτροπή για την επιστημονική αξιολόγηση προϊόντων για τα οποία έχει υποβληθεί αίτηση κεντρικής άδειας κυκλοφορίας σε ολόκληρη την Ευρωπαϊκή Ένωση. Η θετική γνωμοδότηση της CHMP στο στάδιο αυτό έχει υποβληθεί προς έγκριση από την Ευρωπαϊκή Επιτροπή.
Η Janssen αναμένει να λάβει την κανονιστική απόφαση της Ευρωπαϊκής Επιτροπής κατά το τρίτο τρίμηνο του 2011.
Η θετική γνωμοδότηση της CHMP βασίζεται σε δεδομένα μιας μεγάλης, βασικής φάσης 3 τυχαιοποιημένης, διπλά τυφλής κλινικής δοκιμής ελεγχόμενη με εικονικό φάρμακο (μελέτη COU-AA-301). Η μελέτη έδειξε ότι η οξική αμπιρατερόνη, σε συνδυασμό με πρεδνιζόνη ή πρεδνιζολόνη, βελτίωσε τη συνολική επιβίωση ασθενών με προχωρημένο μεταστατικό καρκίνο του προστάτη (CRPC) των οποίων η νόσος είχε σημειώσει πρόοδο κατόπιν χημειοθεραπείας.
Τον Αύγουστο του 2010, η Ανεξάρτητη Επιτροπή Παρακολούθησης Δεδομένων συνέστησε την άρση της τυφλοποίησης της μελέτης κατόπιν προκαθορισμένης ενδιάμεσης ανάλυσης, η οποία έδειξε σημαντική βελτίωση της συνολικής επιβίωσης.
Το Δεκέμβριο του 2010, η αίτηση άδειας κυκλοφορίας υποβλήθηκε στον Ευρωπαϊκό Οργανισμό Φαρμάκων, ενώ η διαδικασία ξεκίνησε τον Ιανουάριο του 2011. Τα βασικά αποτελέσματα της μελέτης COU-AA-301 δημοσιεύθηκαν στο επιστημονικό περιοδικό ‘New England Journal of Medicine’ το Μάιο του 2011.
Τον Απρίλιο του 2011, η οξική αμπιρατερόνη εγκρίθηκε στις ΗΠΑ από τον Ομοσπονδιακό Οργανισμό Τροφίμων και Φαρμάκων (FDA) για χρήση σε συνδυασμό με πρεδνιζόνη ή πρεδνιζολόνη για τη θεραπεία ανδρών με μεταστατικό καρκίνο του προστάτη ανθεκτικού στον ευνουχισμό, οι οποίοι είχαν προηγουμένως υποβληθεί σε χημειοθεραπεία που περιείχε δοσεταξέλη.
‘Θα συνεχίσουμε να συνεργαζόμαστε στενά με τις ευρωπαϊκές υγειονομικές αρχές, προκειμένου να διασφαλίσουμε ότι η οξική αμπιρατερόνη θα καταστεί διαθέσιμη το γρηγορότερο δυνατό σε ασθενείς οι οποίοι πάσχουν από προχωρημένο, μεταστατικό καρκίνο του προστάτη που είναι ανθεκτικός στις συμβατικές ορμονικές θεραπείες και για τους οποίους σήμερα έχουν απομείνει ελάχιστες θεραπευτικές επιλογές’, σχολίασε η Jane Griffiths, Πρόεδρος του Ομίλου Εταιρειών της Janssen για την Ευρώπη, τη Μέση Ανατολή και την Αφρική.
Προχωρημένος μεταστατικός καρκίνος του προστάτη
Ο προχωρημένος μεταστατικός καρκίνος του προστάτη (CRPC) εμφανίζεται, όταν ο καρκίνος του προστάτη παρουσιάζει μετάσταση (εξάπλωση σε άλλα μέρη του σώματος) πέρα από τον προστάτη και η νόσος εξελίσσεται παρότι η τεστοστερόνη του ορού (ανδρογόνα) βρίσκεται κάτω από τα επίπεδα ευνουχισμού.
Το 2008, εκτιμάται ότι διαγνώσθηκαν 370.000 νέα κρούσματα καρκίνου του προστάτη στην Ευρώπη και σχεδόν 90.000 έχασαν τη ζωή τους από τη νόσο.
Οξική αμπιρατερόνη
Τα ανδρογόνα είναι ορμόνες που προωθούν την ανάπτυξη και τη διατήρηση των χαρακτηριστικών του φύλου. Στην περίπτωση του καρκίνου του προστάτη, ωστόσο, τα ανδρογόνα μπορούν να πυροδοτήσουν την αύξηση του όγκου. Η παραγωγή ανδρογόνων συντελείται κατά κύριο λόγο στους όρχεις και στα επινεφρίδια· στους άνδρες με καρκίνο του προστάτη, ο ιστός του όγκου αποτελεί επιπρόσθετη πηγή ανδρογόνων.
Η οξική αμπιρατερόνη είναι ένας αναστολέας βιοσύνθεσης ανδρογόνων που χορηγείται από το στόμα μια φορά την ημέρα και δρα αναστέλλοντας το σύμπλεγμα ενζύμων CYP17, το οποίο είναι απαραίτητο για την παραγωγή ανδρογόνων στις τρεις αυτές πηγές.
Μελέτη COU-AA-301 (www.nejm.org/doi/full/10.1056/NEJMoa1014618)
Αυτή η τυχαιοποιημένη, διπλά τυφλή μελέτη φάσης 3 ελεγχόμενη με εικονικό φάρμακο πραγματοποιήθηκε σε 147 κέντρα 13 χωρών. Η μελέτη αξιολόγησε κατά πόσον η οξική αμπιρατερόνη, σε συνδυασμό με πρεδνιζόνη ή πρεδνιζολόνη, βελτίωσε τη συνολική επιβίωση ασθενών με προχωρημένο μεταστατικό καρκίνο του προστάτη (CRPC) των οποίων η νόσος είχε σημειώσει πρόοδο κατόπιν χημειοθεραπείας.
Ασθενείς με προχωρημένο, μεταστατικό καρκίνο του προστάτη (CPRC) που προηγουμένως λάμβαναν δοσεταξέλη (N=1,195) τυχαιοποιήθηκαν με αναλογία 2:1, ώστε να λάβουν οξική αμπιρατερόνη (1000 mg ημερησίως) σε συνδυασμό με πρεδνιζόνη/πρεδνιζολόνη (5 mg δις ημερησίως) (N = 797), ή εικονικό φάρμακο σε συνδυασμό με πρεδνιζόνη/πρεδνιζολόνη (N = 398).
Το πρωτογενές τελικό σημείο ήταν η συνολική επιβίωση. Τα δευτερεύοντα τελικά σημεία περιελάμβαναν το ποσοστό ανταπόκρισης στο PSA, τη χρονική διάρκεια έως την προοδευτική αύξηση του PSA, και την επιβίωση χωρίς προοδευτική αύξηση βάσει ακτινογραφικών ευρημάτων.
Μετά από παρακολούθηση μέσης διάρκειας 12,8 μηνών, η μελέτη έδειξε ότι η μέση συνολική επιβίωση της ομάδας που έλαβε οξική αμπιρατερόνη σε συνδυασμό με πρεδνιζόνη/πρεδνιζολόνη ήταν 14,8 μήνες έναντι 10,9 μηνών για την ομάδα στην οποία χορηγήθηκε εικονικό φάρμακο σε συνδυασμό με πρεδνιζόνη/πρεδνιζολόνη.
Η θεραπεία με οξική αμπιρατερόνη είχε επίσης ως αποτέλεσμα 35,4% μειωμένο κίνδυνο θανάτου (HR=0,65· 95% CI: 0,54, 0,77·p<0,0001) σε σύγκριση με το εικονικό φάρμακο.
Οι πιο κοινές ανεπιθύμητες αντιδράσεις (μεγαλύτερες ή ίσες με 5%) που αναφέρθηκαν στην κλινική μελέτη, ήταν: αρθρίτιδα ή δυσφορία των αρθρώσεων, υποκαλιαιμία, οίδημα, μυϊκή δυσφορία, έξαψη, διάρροια, λοίμωξη της ουροδόχου κύστης, βήχας, υπέρταση, αρρυθμία, συχνοουρία, νυκτουρία, δυσπεψία και λοίμωξη της άνω αναπνευστικής οδού.
Περισσότερες πληροφορίες διατίθενται στη διεύθυνση http://www.janssen-emea.com/
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
 Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]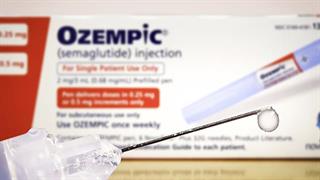 Ozempic και Mounjaro: Ενδείξεις ότι "φρενάρουν" τον καρκίνο
Ozempic και Mounjaro: Ενδείξεις ότι "φρενάρουν" τον καρκίνο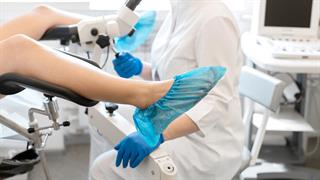 Πάνω από 7 δισ. δολάρια η αγορά των τεστ για καρκίνο του τραχήλου - Kυριαρχεί το τεστ Παπ
Πάνω από 7 δισ. δολάρια η αγορά των τεστ για καρκίνο του τραχήλου - Kυριαρχεί το τεστ Παπ Βασιλακόπουλος: Εντυπωσιακά αποτελέσματα στην επόμενη δεκαετία για τα mRNA εμβόλια κατά του καρκίνου
Βασιλακόπουλος: Εντυπωσιακά αποτελέσματα στην επόμενη δεκαετία για τα mRNA εμβόλια κατά του καρκίνου 3ο Συνέδριο Ασθενών: Ο καρκίνος του μαστού στην Ελλάδα σήμερα
3ο Συνέδριο Ασθενών: Ο καρκίνος του μαστού στην Ελλάδα σήμερα Η Agata Jakoncic στο Most Powerful Women Summit 2026
Η Agata Jakoncic στο Most Powerful Women Summit 2026 Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς