Η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων έδωσε το "πράσινο φως" σε φάρμακο της Dova Pharmaceuticals Inc, που αφορά στη θεραπεία του χαμηλού αριθμού αιμοπεταλίων στους ασθενείς με χρόνια ηπατική νόσο (CLD) που πρόκειται να υποβληθούν σε ιατρική πράξη.
Είμαστε ευχαριστημένοι που ο FDA ενέκρινε το avatrombopag, το οποίο αποτελεί σημαντικό ορόσημο για τη Dova, τους γιατρούς και κυρίως τους ασθενείς", δήλωσε ο Alex C. Sapir, Πρόεδρος και Διευθύνων Σύμβουλος της εταιρείας. "Το φάρμακο είναι η πρώτη από του στόματος χορηγούμενη επιλογή θεραπείας για ασθενείς με CLD, επιτρέποντας στην πλειοψηφία των ασθενών να αποφύγουν τη μετάγγιση αιμοπεταλίων και είμαστε έτοιμοι να το ξεκινήσουμε τον Ιούνιο.
Η θρομβοπενία, η μείωση του αριθμού των αιμοπεταλίων στο αίμα, είναι μια συνηθισμένη επιπλοκή σε ασθενείς με CLD, με την έκτασή της να επιδεινώνεται ανάλογα με τη σοβαρότητα της ηπατικής νόσου.
Υπάρχουν περίπου 70.000 ασθενείς με CLD που έχουν αριθμό αιμοπεταλίων μικρότερο από 50.000 / μL. Αυτοί οι ασθενείς συνήθως απαιτούν 1 έως 3 επεμβατικές διαγνωστικές και θεραπευτικές διαδικασίες ανά έτος. Κάθε μία από αυτές τις διαδικασίες συνεπάγεται κίνδυνο αιμορραγίας. Αν δεν αντιμετωπιστεί αποτελεσματικά, η θρομβοπενία μπορεί να οδηγήσει σε σοβαρή ανεξέλεγκτη αιμορραγία, με αποτέλεσμα παρατεταμένες νοσηλείες και άλλες επιπλοκές μετά τη θεραπεία.
"Αυτό το φάρμακο μπορεί να μειώσει ή να εξαλείψει την ανάγκη για μεταγγίσεις αιμοπεταλίων, οι οποίες συνδέονται με τον κίνδυνο μόλυνσης και άλλων ανεπιθύμητων ενεργειών", δήλωσε ο Richard Pazdur, ενεργός διευθυντής του Γραφείου Αιματολογίας και Ογκολογικών Προϊόντων στο Κέντρο Αξιολόγησης και Έρευνας των Φαρμάκων του FDA.
Ειδήσεις υγείας σήμερα
Πάνω από 3 δισ. ευρώ τα "φέσια" του δημοσίου στην αγορά - Νέα άνοδος
Γύρος επαφών
Η "γκρίζα ζώνη" των ΦΥΚ (1B) και το δύσκολο σταυρόλεξο για το υπουργείο Υγείας
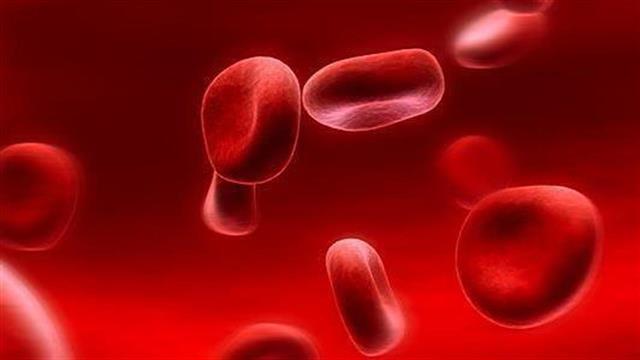
 Ανοσοθρομβοπενία: Νέο μονοκλωνικό αντίσωμα δείχνει σημαντική αποτελεσματικότητα
Ανοσοθρομβοπενία: Νέο μονοκλωνικό αντίσωμα δείχνει σημαντική αποτελεσματικότητα Θρομβωτικό επεισόδιο: Τα πρώιμα σημάδια που δεν πρέπει να αγνοήσουμε
Θρομβωτικό επεισόδιο: Τα πρώιμα σημάδια που δεν πρέπει να αγνοήσουμε Aυτοάνοση Θρομβοπενία: Μια σπάνια αλλά αντιμετωπίσιμη αιματολογική διαταραχή
Aυτοάνοση Θρομβοπενία: Μια σπάνια αλλά αντιμετωπίσιμη αιματολογική διαταραχή Aυτοάνοση Θρομβοπενία: Μια σπάνια αλλά αντιμετωπίσιμη αιματολογική διαταραχή
Aυτοάνοση Θρομβοπενία: Μια σπάνια αλλά αντιμετωπίσιμη αιματολογική διαταραχή Χαμηλά αιμοπετάλια: Συνήθη αίτια θρομβοπενίας
Χαμηλά αιμοπετάλια: Συνήθη αίτια θρομβοπενίας COVID-19: Μελέτη δεν διαπιστώνει αυξημένο γενικό κίνδυνο θρόμβωσης μετά τον εμβολιασμό
COVID-19: Μελέτη δεν διαπιστώνει αυξημένο γενικό κίνδυνο θρόμβωσης μετά τον εμβολιασμό Η "γκρίζα ζώνη" των ΦΥΚ (1B) και το δύσκολο σταυρόλεξο για το υπουργείο Υγείας
Η "γκρίζα ζώνη" των ΦΥΚ (1B) και το δύσκολο σταυρόλεξο για το υπουργείο Υγείας Πάνω από 3 δισ. ευρώ τα "φέσια" του δημοσίου στην αγορά - Νέα άνοδος
Πάνω από 3 δισ. ευρώ τα "φέσια" του δημοσίου στην αγορά - Νέα άνοδος Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς