H βιοφαρμακευτική εταιρεία UCB, με παρουσία σε όλο τον κόσμο, ανακοίνωσε σήμερα τα ενδιάμεσα αποτελέσματα της BE BRIGHT μιας μελέτης ανοιχτής επέκτασης που αξιολόγησε τη μακροχρόνια ασφάλεια, ανεκτικότητα και αποτελεσματικότητα της μπιμεκιζουμάμπης για διάστημα 2 ετών, σε ενήλικους ασθενείς με μέτρια ως σοβαρή Ψωρίαση κατά πλάκας, που είχαν ολοκληρώσει μια εκ των τριών εγκριτικών μελετών Φάσης 3 . Αυτά τα δεδομένα, μαζί με νέα ευρήματα από το κλινικό πρόγραμμα Φάσης 3/3b για τη μπιμεκιζουμάμπη στην Ψωρίαση, ανακοινώθηκαν από την UCB με τη μορφή εννέα περιλήψεων στο 30ο Συνέδριο της Ευρωπαϊκής Ακαδημίας Δερματολογίας και Αφροδισιολογίας (EADV).
Η μπιμεκιζουμάμπη είναι ο πρώτος εκλεκτικός αναστολέας της IL-17A και IL -17F που εγκρίθηκε στην Ευρωπαϊκή Ένωση για τη θεραπεία της μέτριας ως σοβαρής Ψωρίασης κατά πλάκας σε ενήλικους ασθενείς που είναι υποψήφιοι για συστηματική θεραπεία.
“Μετά την πρόσφατη έγκριση της μπιμεκιζουμάμπης στην Ευρώπη, είμαστε στην ευχάριστη θέση να μοιραστούμε τα νέα δεδομένα θεραπείας δύο ετών στο EADV, που υποστηρίζουν την κλινική αξία της μπιμεκιζουμάμπης στη μέτρια έως σοβαρή ψωρίαση. Το εύρος των μακροχρόνιων δεδομένων αποτελεσματικότητας και ασφάλειας που παρουσιάζονται προσφέρουν σημαντικές νέες πληροφορίες για την δερματολογική κοινότητα και αντικατοπτρίζουν τη δέσμευσή μας για βελτίωση της περίθαλψης για άτομα με ψωρίαση,” είπε ο Emmanuel Caeymaex, Εκτελεστικός Αντιπρόεδρος Ανοσολογίας και επικεφαλής ΗΠΑ της UCB.
Τα ενδιάμεσα αποτελέσματα της μελέτης BE BRIGHT που παρουσιάστηκαν στο EADV έδειξαν ότι οι ασθενείς που έλαβαν μπιμεκιζουμάμπη πέτυχαν διατηρήσιμα αποτελέσματα καθαρότητας δέρματος ( PASI 90 PASI 100) για 2 χρόνια με δόση συντήρησης*, και ότι η μπιμεκιζουμάμπη ήταν γενικώς καλά ανεκτή, χωρίς νέα σήματα ασφαλείας. Η μετάβαση στη μπιμεκιζουμάμπη μετά από 24 εβδομάδες χορήγησης ανταλιμουμάμπης στη BE SURE, οδήγησε σε διατηρήσιμη αύξηση των ποσοστών ανταπόκρισης PASI 90 και PASI 100 για διάστημα 2 ετών. Επιπλέον, η μετάβαση σε μπιμεκιζουμάμπη μετά από 52 εβδομάδες θεραπείας με ουστεκινουμάμπη (BE VIVID) οδήγησε σε διατηρήσιμη αύξηση των ποσοστών ανταπόκρισης PASI 100 έως την 100η εβδομάδα. Οι ασθενείς που μεταπήδησαν σε μπιμεκιζουμάμπη μετά από ανεπαρκή ανταπόκριση στην ουστεκινουμάμπη την 52η εβδομάδα, έδειξαν επίσης διατηρήσιμη βελτίωση στα επίπεδα της κάθαρσης του δέρματος (PASI 90 και PASI 100).
“Στην κλινική πρακτική, οι ασθενείς με μέτρια έως σοβαρή ψωρίαση κατά πλάκας μπορεί να χρειαστεί να μεταβούν μεταξύ βιολογικών φαρμάκων για τον βέλτιστο έλεγχο της νόσου τους. Μακροχρόνια αποτελέσματα από τη μελέτη BE SURE και τη μελέτη ανοιχτής επέκτασης BE BRIGHT που ανακοινώθηκαν στο EADV 2021 έδειξαν ότι η μετάβαση από την ανταλιμουμάμπη σε μπιμεκιζουμάμπη, βοήθησε περισσότερους ασθενείς με μέτρια έως σοβαρή ψωρίαση να επιτύχουν και να διατηρήσουν εντελώς καθαρό δέρμα, όπως μετρήθηκε με το δείκτη PASI 100, μετά από δύο χρόνια θεραπείας,” είπε ο καθηγητής Diamant Thaçi, Institute and Comprehensive Center for Inflammation Medicine, University Hospital of Lübeck, Lübeck, Germany.
Μακροχρόνια αποτελέσματα από τις μελέτες BE SURE και την ανοιχτής επέκτασης BE BRIGHT ¥
Αφού τελείωσαν τη μελέτη φάσης 3 BE SURE, οι ασθενείς μπορούσαν να εγγραφούν στη μελέτη ανοιχτής επέκτασης Στους ασθενείς που τυχαιοποιήθηκαν σε μπιμεκιζουμάμπη (320 mg κάθε 4 εβδομάδες [Q4W] για 2 χρόνια), το ποσοστό ανταπόκρισης κατά PASI 90 ήταν 91,2% τόσο στη 16η όσο και στην 104η εβδομάδα. Τα ποσοστά ανταπόκρισης κατά PASI 100 ήταν 62,6% κατά τη 16η εβδομάδα και 72,3% κατά την 104η εβδομάδα. Στους ασθενείς που έλαβαν μπιμεκιζουμάμπη ( 320mg κάθε 4 εβδομάδες για 16 εβδομάδες και στη συνέχεια κάθε 8 εβδομάδες για 2 χρόνια), το ποσοστό των ασθενών που πέτυχαν PASI 90 ήταν 89,4% τη 16η εβδομάδα και 89,7% την 104η. Τα επίπεδα ανταπόκρισης κατά PASI 100 σε αυτή την ομάδα ασθενών ήταν 62,8% τη 16η εβδομάδα και 68,1% την 104η.
Η μετάβαση από ανταλιμουμάμπη σε μπιμεκιζουμάμπη 320mg κάθε 4 εβδομάδες ( Q4W), είχε ως αποτέλεσμα διατηρήσιμα ποσοστά ανταπόκρισης κατά PASI 90 και PASI 100 έως και 2 χρόνια ( 104η εβδομάδα), τα οποία ήταν συγκρίσιμα με τα ποσοστά ανταπόκρισης που παρατηρήθηκαν σε ασθενείς που λάμβαναν συνεχώς μπιμεκιζουμάμπη . Η μπιμεκιζουμάμπη ήταν καλά ανεκτή στη διάρκεια των 2 ετών χωρίς κανένα νέο σήμα ασφάλειας.
Δεδομένα 2 ετών σε ασθενείς της μπιμεκιζουμάμπης που μεταπήδησαν από την ουστεκινουμάμπη ±
Αυτή η ανάλυση συμπεριέλαβε ενήλικες ασθενείς από τη BE VIVID που τυχαιοποιήθηκαν αρχικά σε ουστεκινουμάμπη 45 mg ή 90 mg (ανάλογα με το βάρος τους) τις εβδομάδες 0,4 και στη συνέχεια κάθε 12 εβδομάδες ή σε μπιμεκιζουμάμπη 320 mg κάθε 4 εβδομάδες έως την εβδομάδα 52. Ανάλογα με την ανταπόκριση κατά PASI 90 την εβδομάδα 52, οι ασθενείς που εισήχθησαν στη μελέτη ανοιχτής επέκτασης επανατυχαιοποιηθήκαν σε μπιμεκιζουμάμπη 320 mg κάθε 4 εβδομάδες ή κάθε 8 εβδομάδες.
Κατά την εισαγωγή στη μελέτη ανοιχτής επέκτασης, το 44,9% των ασθενών που έλαβαν ουστεκινουμάμπη και το 73,6% που έλαβαν μπιμεκιζουμάμπη είχαν πετύχει PASI 100. Για όλους τους ασθενείς που μεταπήδησαν από την ουστεκινουμάμπη σε μπιμεκιζουμάμπη, η ανταπόκριση κατά PASI 100 αυξήθηκε στο 65,4 % την 56η εβδομάδα, 78,7 % την 68η εβδομάδα και 69,9 % την 100η εβδομάδα, ποσοστά που ήταν συγκρίσιμα με το ποσοστό ανταπόκρισης που παρατηρήθηκε σε ασθενείς που λάμβαναν συνεχή θεραπεία με μπιμεκιζουμάμπη από την 68η εβδομάδα (75,4%) έως την 100η εβδομάδα (68,8%). Για τους ασθενείς που μεταπήδησαν σε μπιμεκιζουμάμπη μετά από ανεπαρκή ανταπόκριση στην ουστεκινουμάμπη την 52η εβδομάδα, επιτεύχθηκαν υψηλά επίπεδα ανταπόκρισης. Την 56η εβδομάδα, μετά από μία δόση μπιμεκιζουμάμπης, το 77,3 % αυτών των ασθενών πέτυχε PASI 90 και το 40,9 % πέτυχε PASI 100. Η ανταπόκριση αυτή διατηρήθηκε και βελτιώθηκε περαιτέρω την 100η εβδομάδα, με το 84,1 % και 54,5 % των ασθενών να επιτυγχάνουν PASI 90 και PASI 100 , αντίστοιχα. Δεν παρατηρήθηκαν μη αναμενόμενα ευρήματα ασφάλειας σε ασθενείς που μεταπήδησαν από ουστεκινουμάμπη σε μπιμεκιζουμάμπη κατά τη διάρκεια της μελέτης ανοιχτής επέκτασης.
Συγκεντρωτικά αποτελέσματα ασφάλειας 2 ετών θεραπείας στις κλινικές μελέτες Φάσης 2 και 3
Κατά τις μελέτες Φάσης 2 και 3 η συνολική έκθεση της μπιμεκιζουμάμπης ήταν 3109,7 ασθενο-έτη (N=1789). Τα σχετιζόμενα με τη θεραπεία ανεπιθύμητα συμβάντα (TEAEs) που συνέβησαν, σύμφωνα με ένα διορθωμένο ως προς την έκθεση ποσοστό επίπτωσης (EAIR), ήταν 202.4 ανα 100 ασθενο-έτη, τα σοβαρά TEAEs που συνέβησαν, σύμφωνα με το EAIR, ήταν 5.9 νέα περιστατικά ανά 100 ασθενο-έτη και τα TEAEs που οδήγησαν σε διακοπή της θεραπείας ήταν 3.8 νέα περιστατικά ανά 100 ασθενο-έτη. Τα πιο κοινά TEAEs στις μελέτες της μπιμεκιζουμάμπης, φάσης 2 και 3, ήταν η ρινοφαρυγγίτιδα (EAIR: 19.1 νέα περιστατικά ανά 100 ασθενο-έτη), στοματική καντιντίαση (12.6 νέα περιστατικά ανά 100 ασθενο-έτη) και οι λοιμώξεις ανώτερου αναπνευστικού (8.9 νέα περιστατικά ανά 100 ασθενο-έτη). Το διορθωμένο ως προς την έκθεση ποσοστό επίπτωσης (EAIR) για τη στοματική καντιντίαση έδειξε μια μείωση, συγκρινόμενο με τον ένα χρόνο θεραπείας με τη μπιμεκιζουμάμπη (12.6 νέα περιστατικά ανά 100 ασθενο-έτη έναντι 16.4 νέα περιστατικά ανά 100 ασθενο-έτη) και ήταν χαμηλότερο με τη μπιμεκιζουμάμπη χορηγούμενη κάθε 8 εβδομάδες (9,6 ανά 100 ασθενο-έτη), συγκρινόμενο με τη χορήγηση ανά 4 εβδομάδες ( 16,4 ανά 100 ασθενο-έτη). Η πλειονότητα των περιπτώσεων ( 98,5% των ασθενών που παρουσίασαν στοματική καντιντίαση) ήταν ήπιες ή μέτριες και σπάνια οδήγησαν σε διακοπή της μελέτης.
* Η συνιστώμενη δόση τη μπιμεκιζουμάμπης για ενήλικες ασθενείς με ψωρίαση κατά πλάκας είναι 320 mg (χορηγείται ως δύο υποδόριες ενέσεις των 160 mg) την εβδομάδα 0, 4, 8, 12, 16 και στη συνέχεια κάθε οκτώ εβδομάδες. Σε κάποιους ασθενείς με σωματικό βάρος ≥ 120 kg που δεν πετυχαίνουν πλήρη κάθαρση δέρματος τη 16η εβδομάδα, η δοσολογία των 320 mg κάθε τέσσερις εβδομάδες μετά την εβδομάδα 16 μπορεί να βελτιώσει περαιτέρω την ανταπόκριση στη θεραπεία. Στις μελέτες που παρουσιάστηκαν στο EADV 2021, οι ασθενείς έλαβαν δόση συντήρησης μπιμεκιζουμάμπης κάθε 4 ή κάθε 8 εβδομάδες.
¥ Τροποποιημένος καταλογισμός τιμών μη ανταποκριθέντων ασθενών
± Καταλογισμός τιμών μη ανταποκριθέντων ασθενών
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
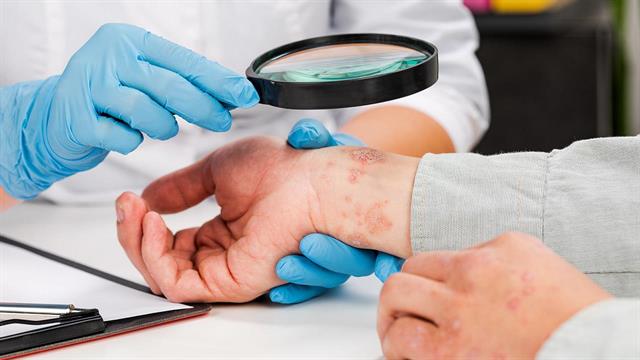
 Ποιες δερματικές παθήσεις βελτιώνονται και ποιες επιδεινώνονται το καλοκαίρι
Ποιες δερματικές παθήσεις βελτιώνονται και ποιες επιδεινώνονται το καλοκαίρι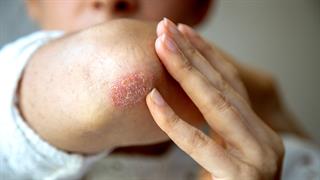 Ψωρίαση: Μύθοι και αλήθειες
Ψωρίαση: Μύθοι και αλήθειες Ο FDA ενέκρινε χάπι για την ψωρίαση
Ο FDA ενέκρινε χάπι για την ψωρίαση Γενικευμένη φλυκταινώδης ψωρίαση: Στη LEO Pharma η άδεια κυκλοφορίας καινοτόμου θεραπείας
Γενικευμένη φλυκταινώδης ψωρίαση: Στη LEO Pharma η άδεια κυκλοφορίας καινοτόμου θεραπείας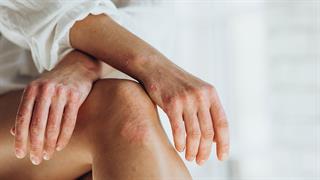 Η ψωρίαση εμποδίζει την ανάπτυξη καρκίνου του δέρματος
Η ψωρίαση εμποδίζει την ανάπτυξη καρκίνου του δέρματος Τύποι δέρματος και η κατάλληλη φροντίδα τους
Τύποι δέρματος και η κατάλληλη φροντίδα τους Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς