Σε επικαιροποίηση των συστάσεων για ανεπιθύμητες ενέργειες των εμβολίων κατά της CoViD της Johhson & Johnson και της AstraZeneca, προχώρησαν οι υπεύθυνοι του Ευρωπαϊκού Οργανισμού Φαρμάκων (ΕΜΑ).
Όπως αναφέρεται σε σημερινό δελτίο του Εθνικού Οργανισμού Φαρμάκων (ΕΟΦ), οι συστάσεις προέρχονται από την Επιτροπή Αξιολόγησης Κινδύνου Φαρμακοεπαγρύπνησης (PRAC) της ΕΜΑ και έχουν ως εξής:
Επικαιροποίηση για τα πολύ σπάνια περιστατικά εγκάρσιας μυελίτιδας. Η PRAC συνέστησε μία αλλαγή στις πληροφορίες προϊόντος για το Vaxzevria (AstraZeneca) και το εμβόλιο έναντι της COVID-19 της Janssen για να συμπεριληφθεί μία προειδοποίηση, με σκοπό την ενημέρωση των επαγγελματιών Υγείας και των ανθρώπων που λαμβάνουν τα εμβόλια.
Aφορά πολύ σπάνια περιστατικά εγκάρσιας μυελίτιδας (ΕΜ) που έχουν αναφερθεί κατόπιν του εμβολιασμού. Η εγκάρσια μυελίτιδα έχει επίσης προστεθεί ως ανεπιθύμητη ενέργεια με άγνωστη συχνότητα.
Είναι μία σπάνια νευρολογική πάθηση που χαρακτηρίζεται από φλεγμονή στη μία ή και στις δύο πλευρές του νωτιαίου μυελού. Μπορεί να προκαλέσει αδυναμία στα χέρια ή στα πόδια, αισθητηριακά συμπτώματα (όπως μυρμήγκιασμα, μούδιασμα, πόνο ή απώλεια της αίσθησης του πόνου) ή προβλήματα με τη λειτουργία της ουροδόχου κύστης ή του εντέρου.
Η Επιτροπή ανασκόπησε τις διαθέσιμες πληροφορίες σε περιστατικά που έχουν αναφερθεί παγκοσμίως, συμπεριλαμβανομένων εκείνων της Ευρωπαϊκής βάσης δεδομένων για εικαζόμενες ανεπιθύμητες ενέργειες (EudraVigilance) και δεδομένων από την επιστημονική βιβλιογραφία και με τα δύο εμβόλια.
Κατέληξε στο συμπέρασμα ότι η αιτιώδης σχέση μεταξύ των δύο εμβολίων και της εγκάρσιας μυελίτιδας είναι τουλάχιστον μία λογική πιθανότητα. Το προφίλ οφέλους - κινδύνου και για τα δύο εμβόλια παραμένει αμετάβλητο.
Οι επαγγελματίες Υγείας θα πρέπει να επαγρυπνούν για σημεία και συμπτώματα της εγκάρσιας μυελίτιδας, επιτρέποντας την έγκαιρη διάγνωση, την υποστηρικτική φροντίδα και τη θεραπεία. Οι άνθρωποι που λαμβάνουν οποιοδήποτε από αυτά τα εμβόλια συνιστάται να αναζητούν άμεση ιατρική φροντίδα εάν αναπτύξουν συμπτώματα αυτής της πάθησης.
Ο EMA θα συνεχίσει να παρακολουθεί στενά αυτό το ζήτημα και θα δημοσιεύσει περαιτέρω εάν νέες πληροφορίες καταστούν διαθέσιμες.
Δεύτερη δόση
Η Επιτροπή του ΕΜΑ συνέστησε να επικαιροποιηθούν οι πληροφορίες προϊόντος για το Vaxzevria (AstraZeneca), για να προστεθούν περισσότερες πληροφορίες σχετικά με πολύ σπάνια περιστατικά θρόμβωσης με θρομβοπενία (TTS), που εμφανίστηκαν κατόπιν του εμβολιασμού.
Μία ανασκόπηση των συγκεντρωτικών δεδομένων επεσήμανε ότι η πλειονότητα των εικαζόμενων περιστατικών TTS αναφέρθηκαν παγκοσμίως μετά από τη χορήγηση της πρώτης δόσης.
Έχουν παρατηρηθεί λιγότερα περιστατικά μετά από τη δεύτερη δόση. Στην πραγματικότητα, από τα 1.809 θρομβοεμβολικά περιστατικά με θρομβοπενία που αναφέρθηκαν παγκοσμίως, τα 1.643 αναφέρθηκαν μετά από την πρώτη δόση και τα 166 μετά από τη δεύτερη δόση.
Όσον αφορά τις τρέχουσες πληροφορίες προϊόντος, η χορήγηση της δεύτερης δόσης του Vaxzevria αντενδείκνυται σε ανθρώπους που παρουσίασαν TTS μετά από εμβολιασμό με αυτό το εμβόλιο.
Πηγές:
ΕΟΦ
Ειδήσεις υγείας σήμερα
Οι Φυσικοθεραπευτές ζητούν την άμεση ένταξή τους στα Βαρέα και Ανθυγιεινά Επαγγέλματα
Χάπι της AstraZeneca για την παχυσαρκία φέρνει ανατροπές
Εμ. Ροηλίδης: Διεθνής διάκριση για τον καθηγητή Παιδιατρικής λοιμωξιολογίας

 ΕΟΔΥ: 1 θάνατος από γρίπη - σε αποδρομή CoViD και RSV
ΕΟΔΥ: 1 θάνατος από γρίπη - σε αποδρομή CoViD και RSV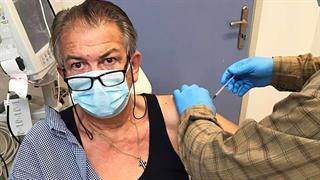 ΕΜΑ: Συνιστά επικαιροποίηση των εμβολίων κατά της CoViD, ώστε να στοχεύουν την παραλλαγή XFG
ΕΜΑ: Συνιστά επικαιροποίηση των εμβολίων κατά της CoViD, ώστε να στοχεύουν την παραλλαγή XFG ΕΟΔΥ: Χαμηλή διασπορά γρίπης, κορωνοϊού - Ένας θάνατος ασθενή με CoViD - Σε ύφεση και ο RSV
ΕΟΔΥ: Χαμηλή διασπορά γρίπης, κορωνοϊού - Ένας θάνατος ασθενή με CoViD - Σε ύφεση και ο RSV ΕΟΔΥ: Λήξη συναγερμού για τις ιώσεις του αναπνευστικού - Υποχωρούν γρίπη, RSV, κορωνοϊός
ΕΟΔΥ: Λήξη συναγερμού για τις ιώσεις του αναπνευστικού - Υποχωρούν γρίπη, RSV, κορωνοϊός Πώς το εμβόλιο για τον RSV οδήγησε στο εμβόλιο για την CoViD
Πώς το εμβόλιο για τον RSV οδήγησε στο εμβόλιο για την CoViD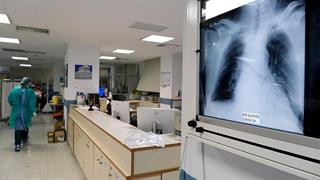 ΕΟΔΥ: Αύξηση στα κρούσματα RSV, σε αποδρομή CoViD - γρίπη
ΕΟΔΥ: Αύξηση στα κρούσματα RSV, σε αποδρομή CoViD - γρίπη Εμ. Ροηλίδης: Διεθνής διάκριση για τον καθηγητή Παιδιατρικής λοιμωξιολογίας
Εμ. Ροηλίδης: Διεθνής διάκριση για τον καθηγητή Παιδιατρικής λοιμωξιολογίας White paper από Ομοσπονδίες Διαβήτη και Οφθαλμολογικών δυσλειτουργιών
White paper από Ομοσπονδίες Διαβήτη και Οφθαλμολογικών δυσλειτουργιών Το μέλλον της εξατομικευμένης ιατρικής: Τα γονίδια καθορίζουν τη θεραπεία
Το μέλλον της εξατομικευμένης ιατρικής: Τα γονίδια καθορίζουν τη θεραπεία Χάπι της AstraZeneca για την παχυσαρκία φέρνει ανατροπές
Χάπι της AstraZeneca για την παχυσαρκία φέρνει ανατροπές Ι. Καβαλιώτης: Αποχαιρετισμός σε έναν δάσκαλο των παιδιατρικών λοιμώξεων
Ι. Καβαλιώτης: Αποχαιρετισμός σε έναν δάσκαλο των παιδιατρικών λοιμώξεων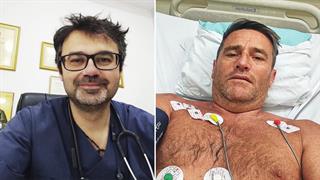 Χαλκιδική: Ο Μάρτιν βγήκε από τη ΜΕΘ και βρήκε τον γιατρό που τού έσωσε τη ζωή
Χαλκιδική: Ο Μάρτιν βγήκε από τη ΜΕΘ και βρήκε τον γιατρό που τού έσωσε τη ζωή Εγκαίνια 2 νέων αξονικών τομογράφων και της νέας Καρδιολογικής Κλινικής στο Γενικό Ογκολογικό Νοσοκομείο Κηφισιάς ''Οι Άγιοι Ανάργυροι''
Εγκαίνια 2 νέων αξονικών τομογράφων και της νέας Καρδιολογικής Κλινικής στο Γενικό Ογκολογικό Νοσοκομείο Κηφισιάς ''Οι Άγιοι Ανάργυροι'' Τι αλλάζει από τον Ιούλιο στα απογευματινά ιατρεία των νοσοκομείων [εγκύκλιος]
Τι αλλάζει από τον Ιούλιο στα απογευματινά ιατρεία των νοσοκομείων [εγκύκλιος] Δ. Ματθαίος: Τρία ελπιδοφόρα νέα στη μάχη κατά του καρκίνου
Δ. Ματθαίος: Τρία ελπιδοφόρα νέα στη μάχη κατά του καρκίνου Προσλήψεις παθολόγων στη Δράμα μέσω Θεσσαλονίκης;
Προσλήψεις παθολόγων στη Δράμα μέσω Θεσσαλονίκης; 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου Αρχή Προστασίας Προσωπικών Δεδομένων: Κόκκινη κάρτα στο υπουργείο Εσωτερικών για τα βιομετρικά στοιχεία
Αρχή Προστασίας Προσωπικών Δεδομένων: Κόκκινη κάρτα στο υπουργείο Εσωτερικών για τα βιομετρικά στοιχεία