Οι εταιρείες Biontech και η Pfizer ανακοίνωσαν την Παρασκευή ότι υπέβαλαν αίτηση στον Ευρωπαϊκό Οργανισμό Φαρμάκων (ΕΜΑ) για την επικαιροποίηση της υπό όρους άδειας κυκλοφορίας για το εμβόλιο Comirnaty που βασίζεται στο mRNA Covid-19.
Μέχρι σήμερα, το προϊόν διαθέτει άδεια κυκλοφορίας υπό όρους για ενήλικες και παιδιά ηλικίας δώδεκα ετών και άνω σε δόση 30 μg και για παιδιά ηλικίας 5 - 11 ετών με δοσολογία 10 μg.
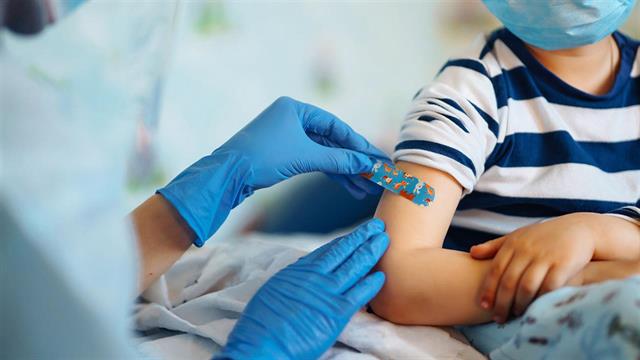
Η μικρότερη ηλικιακή ομάδα παιδιών ηλικίας 6 μηνών - 4 ετών πρέπει να λαμβάνει 3 μg δραστικής ουσίας ανά εμβολιασμό.
Σε αντίθεση με τα μεγαλύτερα παιδιά και τους ενήλικες, στην περίπτωση αυτή ζητείται άμεσα έγκριση για ένα πρόγραμμα εμβολιασμού τριών δόσεων: δύο δόσεις σε διάστημα τριών εβδομάδων και μια τρίτη δόση στην ίδια δοσολογία τουλάχιστον δύο μήνες μετά τη χορήγηση της δεύτερης δόσης. Στην προκειμένη περίπτωση, η τρίτη δόση θα αποτελεί μέρος της βασικής ανοσοποίησης (σειρά πρωτογενών εμβολιασμών).
Η σχετική υποκείμενη μελέτη διεξήχθη σε μια εποχή που η παραλλαγή Omicron ήταν ήδη η κυρίαρχη παραλλαγή του ιού.
Μετά τη χορήγηση της τρίτης δόσης του εμβολίου, παρατηρήθηκαν ισχυρές ανοσολογικές αποκρίσεις στα παιδιά κάτω των πέντε ετών, ενώ το προφίλ ασφάλειας ήταν ευνοϊκό και συγκρίσιμο με το προφίλ του εικονικού φαρμάκου, αναφέρθηκε χαρακτηριστικά.
"Δεν παρατηρήθηκαν προειδοποιήσεις ασφάλειας και η συχνότητα των ανεπιθύμητων ενεργειών που παρατηρήθηκαν σε παιδιά ηλικίας έξι μηνών έως κάτω των πέντε ετών ήταν γενικά χαμηλότερη από ό,τι σε παιδιά ηλικίας πέντε ετών έως κάτω των 12 ετών", αναφέρουν οι εταιρείες.
Στις ΗΠΑ, το Comirnaty με δοσολογία 3 μg έχει ήδη λάβει έγκριση έκτακτης ανάγκης για αυτή την ηλικιακή ομάδα από τον Ιούνιο.
Εφόσον δεν υπάρξουν επιφυλάξεις από τον EMA, το εμβόλιο για βρέφη θα μπορούσε, επομένως, να είναι ενδεχομένως διαθέσιμο πριν από το φθινόπωρο για την ανοσοποίηση των παιδιών σε βρεφονηπιακούς και παιδικούς σταθμούς κατά του SARS-CoV-2.
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
 Μήνυμα υπέρ της πρόληψης και του εμβολιασμού από Άδωνι Γεωργιάδη και Ειρήνη Αγαπηδάκη
Μήνυμα υπέρ της πρόληψης και του εμβολιασμού από Άδωνι Γεωργιάδη και Ειρήνη Αγαπηδάκη Ενημερωτική εκστρατεία για τον διά βίου εμβολιασμό
Ενημερωτική εκστρατεία για τον διά βίου εμβολιασμό Προστασία των παιδιών από πνευμονιόκοκκο - Η αξία του εμβολιασμού
Προστασία των παιδιών από πνευμονιόκοκκο - Η αξία του εμβολιασμού EMA: Συμβουλευτική ομάδα για αύξηση της εμπιστοσύνης των πολιτών στα εμβόλια
EMA: Συμβουλευτική ομάδα για αύξηση της εμπιστοσύνης των πολιτών στα εμβόλια Ο ΠΦΣ για την Παγκόσμια Εβδομάδα Εμβολιασμών
Ο ΠΦΣ για την Παγκόσμια Εβδομάδα Εμβολιασμών Ο εμβολιασμός σώζει έξι ζωές το λεπτό, κάθε μέρα, επί πέντε δεκαετίες
Ο εμβολιασμός σώζει έξι ζωές το λεπτό, κάθε μέρα, επί πέντε δεκαετίες Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς