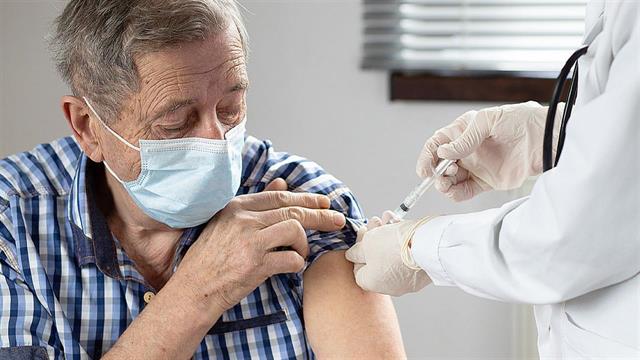
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) εισηγείται την κυκλοφορία στην Ευρωπαϊκή Ένωση του Arexvy, του πρώτου εμβολίου για προστασία ενηλίκων ηλικίας 60 ετών και άνω έναντι της νόσου του κατώτερου αναπνευστικού που προκαλείται από τον αναπνευστικό συγκυτιακό ιό (RSV).
Ο RSV είναι ένας κοινός αναπνευστικός ιός που συνήθως προκαλεί ήπια συμπτώματα που μοιάζουν με κρυολόγημα. Οι περισσότεροι άνθρωποι αναρρώνουν μέσα σε μία έως δύο εβδομάδες, αλλά η νόσηση μπορεί να είναι σοβαρή σε ευάλωτα άτομα, συμπεριλαμβανομένων των ηλικιωμένων και εκείνων με πνευμονική ή καρδιακή νόσο και διαβήτη. Στην Ευρώπη, ο RSV προκαλεί περίπου 250.000 νοσηλείες και 17.000 θανάτους νοσηλευόμενων κάθε χρόνο σε άτομα ηλικίας 65 ετών και άνω.
Το Arexvy περιέχει μια τροποποιημένη έκδοση της γλυκοπρωτεΐνης επιφάνειας σύντηξης RSV. Αυτή η πρωτεΐνη είναι απαραίτητη για να μολύνει το σώμα ο RSV και είναι επίσης ο κύριος στόχος των αντισωμάτων που παράγονται για την καταπολέμηση της λοίμωξης. Το εμβόλιο περιέχει επίσης ένα ανοσοενισχυτικό, μια ουσία που βοηθά στην ενίσχυση της ανοσολογικής απόκρισης στο εμβόλιο. Όταν ένα άτομο λαμβάνει το εμβόλιο, το ανοσοποιητικό του σύστημα δημιουργεί συγκεκριμένα αντισώματα και Τ κύτταρα που βοηθούν στην πρόληψη της μόλυνσης από RSV.
Το Arexvy αξιολογήθηκε στο πλαίσιο του μηχανισμού ταχείας αξιολόγησης του EMA επειδή η πρόληψη της λοίμωξης από RSV στον ηλικιωμένο πληθυσμό θεωρείται μείζονος σημασίας για τη δημόσια υγεία.
Η γνώμη της επιτροπής για τα ανθρώπινα φάρμακα (CHMP) του EMA βασίζεται σε δεδομένα από μια τυχαιοποιημένη, ελεγχόμενη με εικονικό φάρμακο δοκιμή σε 25.000 ενήλικες σε 17 χώρες. Τα αποτελέσματα έδειξαν εκτιμώμενη προστασία 83% έναντι LRTD επιβεβαιωμένης από RSV για τουλάχιστον έξι μήνες. Οι πιο συχνές ανεπιθύμητες ενέργειες που αναφέρθηκαν ήταν πονοκέφαλος, κόπωση, μυϊκός πόνος, πόνος στις αρθρώσεις και πόνος στο σημείο της ένεσης.
Η μελέτη είναι ακόμη σε εξέλιξη και θα χρησιμοποιηθεί για την αξιολόγηση της αποτελεσματικότητας μιας εφάπαξ δόσης Arexvy σε πολλαπλές εποχές και της ανάγκης για εκ νέου εμβολιασμό, καθώς και για την παρακολούθηση του προφίλ ασφάλειάς του.
Η γνώμη της CHMP είναι ένα ενδιάμεσο βήμα στην πορεία της Arexvy προς την πρόσβαση ασθενών. Η γνώμη θα σταλεί τώρα στην Ευρωπαϊκή Επιτροπή για την έκδοση απόφασης σχετικά με άδεια κυκλοφορίας σε επίπεδο ΕΕ. Μετά τη χορήγηση άδειας κυκλοφορίας, οι αποφάσεις σχετικά με την τιμή και την αποζημίωση θα λαμβάνονται σε επίπεδο κάθε κράτους μέλους, λαμβάνοντας υπόψη τον πιθανό ρόλο/χρήση αυτού του φαρμάκου στο πλαίσιο του εθνικού συστήματος Υγείας αυτής της χώρας.
Πηγές:
ΕΜΑ
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
 Μήνυμα υπέρ της πρόληψης και του εμβολιασμού από Άδωνι Γεωργιάδη και Ειρήνη Αγαπηδάκη
Μήνυμα υπέρ της πρόληψης και του εμβολιασμού από Άδωνι Γεωργιάδη και Ειρήνη Αγαπηδάκη Ενημερωτική εκστρατεία για τον διά βίου εμβολιασμό
Ενημερωτική εκστρατεία για τον διά βίου εμβολιασμό Εμβόλια ενηλίκων: Γιατί η προστασία δεν σταματά στην παιδική ηλικία
Εμβόλια ενηλίκων: Γιατί η προστασία δεν σταματά στην παιδική ηλικία EMA: Συμβουλευτική ομάδα για αύξηση της εμπιστοσύνης των πολιτών στα εμβόλια
EMA: Συμβουλευτική ομάδα για αύξηση της εμπιστοσύνης των πολιτών στα εμβόλια Ο ΠΦΣ για την Παγκόσμια Εβδομάδα Εμβολιασμών
Ο ΠΦΣ για την Παγκόσμια Εβδομάδα Εμβολιασμών Ο εμβολιασμός σώζει έξι ζωές το λεπτό, κάθε μέρα, επί πέντε δεκαετίες
Ο εμβολιασμός σώζει έξι ζωές το λεπτό, κάθε μέρα, επί πέντε δεκαετίες Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς