Η Sanofi και η Regeneron Pharmaceuticals, Inc. ανακοίνωσαν ότι οι δύο μελέτες Φάσης 3 (ελεγχόμενες με εικονικό φάρμακο) για την αξιολόγηση του νέου υπό δοκιμή μονοκλωνικού αντισώματος dupilumab σε ενήλικες ασθενείς με ανεπαρκώς ελεγχόμενη μέτρια-έως-σοβαρή ατοπική δερματίτιδα (ΑΔ) πέτυχαν το πρωτεύον καταληκτικό σημείο. Στις μελέτες, γνωστές ως LIBERTY AD SOLO 1 και SOLO 2, η μονο-θεραπεία με χορήγηση dupilumab ως μονοθεραπεία βελτίωσε σημαντικά παραμέτρους όπως η συνολική βαρύτητα της νόσου, η υποχώρηση των δερματικών εκδηλώσεων, ο κνησμός, η ποιότητα ζωής και η ψυχική υγεία των ασθενών.
«Είναι οι πρώτες μελέτες Φάσης 3 μιας συστηματικής θεραπείας που τεκμηριώνουν σημαντική βελτίωση στα συμπτώματα της μέτριας έως σοβαρής ατοπικής δερματίτιδας, μιας χρόνιας, φλεγμονώδους νόσου που ταλαιπωρεί πάνω από ένα εκατομμύριο Αμερικανούς», ανέφερε ο κ. George Yancopoulos, M.D., Ph.D, Chief Scientific Officer, Regeneron και President of Regeneron Laboratories. «Αυτά τα δεδομένα παρέχουν ισχυρές αποδείξεις για το ότι η οδός σηματοδότησης που σχετίζεται με τις κυτοκίνες IL-4 και IL-13 αποτελεί ένα καθοριστικό παράγοντα δημιουργίας της φλεγμονής στην ατοπική δερματίτιδα. Το Dupilumab είναι το πρώτο υπό ανάπτυξη μόριο μιας νέας κατηγορίας ανοσοθεραπειών. Στις Κλινικές δοκιμές διάρκειας 16 εβδομάδων, το dupilumab εμπόδισε τη μη φυσιολογική ενεργοποίηση της συγκεκριμένης οδού, γεγονός που καθόρισε τη σημαντική αποτελεσματικότητα χωρίς την εμφάνιση ανεπιθύμητων ενεργειών σχετιζόμενων με ανοσοκαταστολή. Συνεχίζουμε να αξιολογούμε το ρόλο των κυτοκινών IL-4 και IL-13 σε συναφείς φλεγμονώδεις καταστάσεις, συμπεριλαμβανομένου του άσθματος και της ρινικής πολυποδίασης, όπου κλινικά προγράμματα με βάση το dupilumab βρίσκονται σε εξέλιξη.»
«Δεν υπάρχουν εγκεκριμένες συστηματικές θεραπείες στις ΗΠΑ για ασθενείς με μέτρια έως σοβαρή ατοπική δερματίτιδα, γεγονός που υπογραμμίζει τη σημαντική ακάλυπτη θεραπευτική ανάγκη. Τα αποτελέσματα αυτά φέρνουν ελπίδα στους ασθενείς με ατοπική δερματίτιδα, πολλοί εκ των οποίων υποφέρουν για χρόνια», τονίζει ο κ. Elias Zerhouni, M.D., President Global R & D, Sanofi. «Στις ΗΠΑ, όπου το dupilumab έχει ήδη χαρακτηριστεί από την Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) ως Καινοτόμα Θεραπεία για την ατοπική δερματίτιδα, σκοπεύουμε να υποβάλλουμε το φάκελο έγκρισης προς τις αρχές το τρίτο τρίμηνο του 2016 και συγχρόνως θα εργαστούμε για να παρέχουμε αυτή την καινοτόμα θεραπεία όσο το δυνατόν γρηγορότερα στους ασθενείς.»
Συνολικά 1.379 ενήλικες ασθενείς με μέτρια έως σοβαρή ατοπική δερματίτιδα συμπεριελήφθησαν στις πανομοιότυπα σχεδιασμένες μελέτες SOLO 1 και SOLO 2. Οι ασθενείς επιλέχθηκαν με βάση τον ανεπαρκή έλεγχο των συμπτωμάτων μετά από τοπική θεραπεία ή εάν δε συστήνονταν η χορήγηση τοπικής θεραπείας. Οι ασθενείς αξιολογήθηκαν με την 5-βαθμια κλίμακα Συνολικής Αξιολόγησης του Ερευνητή (Investigator’s Global Assessment - IGA), η οποία περιελάμβανε τις βαθμίδες από το 0 (χωρίς δερματικές βλάβες) έως το 4 (σοβαρή δερματική βλάβη). Σύμφωνα με τα κριτήρια ένταξης μόνο ασθενείς με αξιολόγηση IGA 3 ή 4 εντάχθηκαν στις μελέτες. Οι ασθενείς επίσης αξιολογήθηκαν με βάση το δείκτη EASI (Eczema Area and Severity Index – Δείκτης Βαρύτητας του εκζέματος) καθώς και με άλλα κριτήρια. Οι ασθενείς τυχαιοποιήθηκαν σε τρεις ομάδες θεραπείας: 300 mg dupilumab υποδόρια μια φορά εβδομαδιαίως, 300 mg dupilumab υποδόρια κάθε δύο εβδομάδες ή εικονικό φάρμακο για 16 εβδομάδες μετά από τη χορήγηση αρχικής δόσης dupilumab 600 mg υποδόρια, ή εικονικού φαρμάκου. Τα αποτελέσματα μετά από 16 εβδομάδες συνοψίζονται στα εξής:
- στις μελέτες SOLO 1 και SOLO 2, το 37% και το 36% των ασθενών αντίστοιχα, που έλαβαν 300 mg dupilumab ανά εβδομάδα και το 38% και 36% των ασθενών που έλαβαν 300 mg dupilumab κάθε δύο εβδομάδες πέτυχαν πλήρη υποχώρηση ή σχεδόν πλήρη υποχώρηση των δερματικών βλαβών (IGA 0 ή 1), σε σύγκριση με το 10% και το 8.5% των ασθενών που έλαβαν το εικονικό φάρμακο (p<0.0001). Αυτό ήταν το πρωτεύον καταληκτικό σημείο της μελέτης στις ΗΠΑ.
- το ποσοστό βελτίωσης βάσει του δείκτη EASI από την έναρξη της μελέτης ήταν 72% και 69% αντίστοιχα για τους ασθενείς που έλαβαν το δοσολογικό σχήμα των 300 mg ανά εβδομάδα, και 72% και 67% για τους ασθενείς που έλαβαν το δοσολογικό σχήμα των 300 mg κάθε δύο εβδομάδες, σε σύγκριση με το 38% και το 31% για τους ασθενείς με εικονικό φάρμακο (p<0.0001).
- 52.5% και 48% των ομάδων ασθενών που έλαβαν το δοσολογικό σχήμα των 300 mg εβδομαδιαίως, και το 51% και 44% των ομάδων ασθενών που έλαβαν το σχήμα των 300 mg κάθε δύο εβδομάδες σημείωσαν βελτίωση 75% βάσει του δείκτη EASI σε σύγκριση με το 15% και το 12% των ασθενών που έλαβαν το εικονικό φάρμακο (p<0.0001). Αυτό ήταν το δευτερεύον καταληκτικό σημείο των μελετών στις ΗΠΑ και ένα από τα πρωτεύοντα καταληκτικά σημεία στην Ευρώπη.
Κατά την περίοδο των 16 εβδομάδων θεραπείας, το συνολικό ποσοστό ανεπιθύμητων ενεργειών ήταν συγκρίσιμο μεταξύ των ομάδων με dupilumab (65%-73%) και των ομάδων με εικονικό φάρμακο (65%-72%). Το 88%-94% των ασθενών στις ομάδες του dupilumab ολοκλήρωσε τη θεραπεία έναντι 80.5%-82% στην ομάδα του εικονικού φαρμάκου. Το ποσοστό των σοβαρών ανεπιθύμητων ενεργειών ήταν 1%-3% για το dupilumab και 5%-6% για το εικονικό φάρμακο. Η συχνότητα εμφάνισης σοβαρών λοιμώξεων στις ομάδες με εικονικό φάρμακο ήταν υψηλότερη και στις δύο μελέτες (0.5%-1% με dupilumab και 2%-3% με εικονικό φάρμακο). Οι πιο συχνά αναφερόμενες ανεπιθύμητες ενέργειες στη θεραπεία με dupilumab και στις δύο μελέτες ήταν αντιδράσεις στο σημείο έγχυσης (10%-20% με dupilumab, 7%-8% με εικονικό φάρμακο) και επιπεφυκίτιδα (7%-12% με dupilumab, 2% με εικονικό φάρμακο). Περίπου 26% των ασθενών και στις δύο μελέτες ανέφερε ιστορικό αλλεργικής επιπεφυκίτιδας κατά την έναρξη της μελέτης. Κανένας ασθενής δεν διέκοψε τη θεραπεία λόγω αντίδρασης στο σημείο έγχυσης και μόνο ένας ασθενής διέκοψε τη θεραπεία λόγω επιπεφυκίτιδας.
Περισσότερο αναλυτικά και λεπτομερή αποτελέσματα για τις μελέτες SOLO 1 και SOLO 2 θα παρουσιαστούν σε επόμενο ιατρικό συνέδριο.
Η Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) χαρακτήρισε το dupilumab ως Καινοτόμο Θεραπεία για την ατοπική δερματίτιδα το Νοέμβριο, 2014. Το dupilumab είναι επί του παρόντος υπό κλινική ανάπτυξη και η ασφάλεια και η αποτελεσματικότητα του δεν έχουν αξιολογηθεί πλήρως από καμία ρυθμιστική αρχή.
Το κλινικό πρόγραμμα Φάσης 3 LIBERTY AD περιλαμβάνει πέντε μελέτες σε ασθενείς με μέτρια έως σοβαρή ατοπική δερματίτιδα παγκοσμίως.
Σχετικά με την Ατοπική Δερματίτιδα
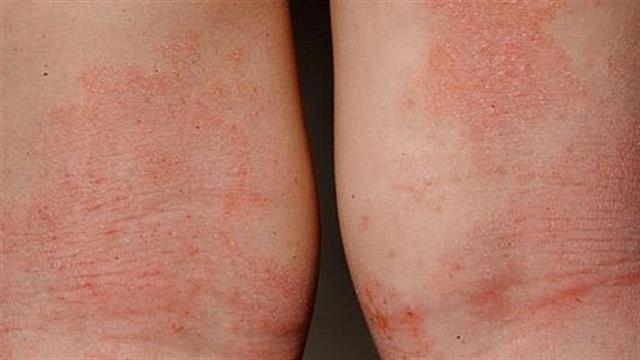
Η ατοπική δερματίτιδα - μια σοβαρή μορφή εκζέματος - είναι μια χρόνια, κνησμώδης, φλεγμονώδης νόσος του δέρματος που μπορεί να εκδηλωθεί σε οποιοδήποτε μέρος του σώματος.Παρόλο που τα συμπτώματα είναι ορατά στην επιφάνεια του δέρματος, η ατοπική δερματίτιδα χαρακτηρίζεται από συστηματική φλεγμονή. Η ατοπική δερματίτιδα παρουσιάζεται σχεδόν σε 7-8 εκατομμύρια ενηλίκων στις ΗΠΑ και στο 1% έως 3% των ενηλίκων παγκοσμίως. Σύμφωνα με μια έρευνα 200 ιατρών, υπάρχουν σχεδόν 1,6 εκατομμύρια ασθενών στις ΗΠΑ που έχουν διαγνωστεί με μέτρια έως σοβαρή ατοπική δερματίτιδα και έχουν υποβληθεί σε θεραπεία χωρίς σημαντική βελτίωση.Περίπου το 70% των ανθρώπων με ατοπική δερματίτιδα έχουν οικογενειακό ιστορικό ατοπικών ασθενειών, όπως άσθμα ή αλλεργική ρινίτιδα. Ο έντονος κνησμός, η φαγούρα και οι δερματικές βλάβες που σχετίζονται με τη νόσο μπορεί μερικές φορές να οδηγήσουν σε λοιμώξεις, που προκαλούνται από βακτήρια, όπως το Staphylococcus aureus. Επιπρόσθετα, τα σωματικά συμπτώματα της νόσου ενδέχεται να προκαλέσουν άγχος, κατάθλιψη και αίσθημα κοινωνικής απομόνωσης.
Ειδήσεις υγείας σήμερα
Επιστρέφει σήμερα ο Έλληνας που ήταν στο κρουαζιερόπλοιο με τον χανταϊό
Κάποιες σκέψεις για τη γιορτή της μητέρας...
Αντιφλεγμονώδεις τροφές που και πάλι θέλουν προσοχή
 Το στρες συνδέεται με ατοπική δερματίτιδα
Το στρες συνδέεται με ατοπική δερματίτιδα Ατοπική δερματίτιδα: Ανακαλύφθηκε ο μηχανισμός του κνησμού
Ατοπική δερματίτιδα: Ανακαλύφθηκε ο μηχανισμός του κνησμού Ο FDA ενέκρινε κρέμα για την ατοπική δερματίτιδα στα παιδιά
Ο FDA ενέκρινε κρέμα για την ατοπική δερματίτιδα στα παιδιά Δείτε την Ατοπική Δερματίτιδα όπως πραγματικά είναι
Δείτε την Ατοπική Δερματίτιδα όπως πραγματικά είναι Ατοπική δερματίτιδα: Μπορεί ένα εμβόλιο να τη θεραπεύσει;
Ατοπική δερματίτιδα: Μπορεί ένα εμβόλιο να τη θεραπεύσει; Αντιυπερτασικά συνδέονται με την ατοπική δερματίτιδα στους ηλικιωμένους [μελέτη]
Αντιυπερτασικά συνδέονται με την ατοπική δερματίτιδα στους ηλικιωμένους [μελέτη] Αντιφλεγμονώδεις τροφές που και πάλι θέλουν προσοχή
Αντιφλεγμονώδεις τροφές που και πάλι θέλουν προσοχή Επιστρέφει σήμερα ο Έλληνας που ήταν στο κρουαζιερόπλοιο με τον χανταϊό
Επιστρέφει σήμερα ο Έλληνας που ήταν στο κρουαζιερόπλοιο με τον χανταϊό Iδέες για πρωινό για άτομα με υψηλή χοληστερόλη
Iδέες για πρωινό για άτομα με υψηλή χοληστερόλη Κάποιες σκέψεις για τη γιορτή της μητέρας...
Κάποιες σκέψεις για τη γιορτή της μητέρας... Πώς προχωρά η συγκεντροποίηση της αιμοδοσίας-Ποια νοσοκομεία έχουν συνδεθεί με το ΕΚΕΑ
Πώς προχωρά η συγκεντροποίηση της αιμοδοσίας-Ποια νοσοκομεία έχουν συνδεθεί με το ΕΚΕΑ Νοσοκομείο Καβάλας: Το θερμό επεισόδιο του διοικητή με δύο γιατρούς και οι συλλήψεις
Νοσοκομείο Καβάλας: Το θερμό επεισόδιο του διοικητή με δύο γιατρούς και οι συλλήψεις Οι χειρότερες τροφές για πριν τον ύπνο
Οι χειρότερες τροφές για πριν τον ύπνο Οι δύσκολες ιατρικές αποφάσεις στο τέλος της ζωής - Παίζει ρόλο η ηλικία του ασθενή;
Οι δύσκολες ιατρικές αποφάσεις στο τέλος της ζωής - Παίζει ρόλο η ηλικία του ασθενή; Επικροτούν οι παθολόγοι την εξαίρεση του προσωπικού γιατρού από επισκέψεις κατ΄ οίκον
Επικροτούν οι παθολόγοι την εξαίρεση του προσωπικού γιατρού από επισκέψεις κατ΄ οίκον Aποσύρσεις φαρμάκων και αποχωρήσεις στελεχών
Aποσύρσεις φαρμάκων και αποχωρήσεις στελεχών Καθηγητής Τσακρής: Πόσο επικίνδυνος είναι ο χανταϊός
Καθηγητής Τσακρής: Πόσο επικίνδυνος είναι ο χανταϊός Προκήρυξη 1.131 θέσεων ειδικευμένων ιατρών ΕΣΥ επί θητεία σε δημόσιες δομές
Προκήρυξη 1.131 θέσεων ειδικευμένων ιατρών ΕΣΥ επί θητεία σε δημόσιες δομές