H δεύτερη ένδειξη του isatuximab για τη θεραπεία ενηλίκων ασθενών με υποτροπιάζον πολλαπλούν μυέλωμα, εγκρίθηκε από την Ευρωπαϊκή Επιτροπή. Αυτή η δεύτερη έγκριση του σκευάσματος είναι σε συνδυασμό με την καρφιλζομίμπη και τη δεξαμεθαζόνη για ενήλικες ασθενείς που έχουν λάβει τουλάχιστον μία προηγούμενη θεραπεία, μαζί με ένα πρότυπο θεραπευτικής αγωγής σε λιγότερο από 12 μήνες.
O Philippe Moreau από το Πανεπιστημιακό Νοσοκομείο της Νάντης, στο Τμήμα Αιματολογίας είπε: ‘’Καθώς δεν υπάρχει θεραπεία για πολλαπλούν μυέλωμα και οι ασθενείς συχνά αντιμετωπίζουν υποτροπή νόσου, πρέπει να επιμείνουμε στην επιδίωξή μας για πρόσθετες θεραπευτικές επιλογές. Σχεδόν το 30% των ασθενών που έλαβαν θεραπεία με isatuximab ανταποκρίθηκαν."
Αυτή η τελευταία έγκριση ακολουθεί την αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων (FDA) που ενέκρινε το σκεύασμα για παρόμοια ένδειξη τον Μάρτιο του 2021.
Ο επικεφαλής της Sanofi Oncology and Pediatric Innovation Global Development, Peter C Adamson, δήλωσε: «Η έγκριση του isatuximab από την Ευρωπαϊκή Επιροπή, σε συνδυασμό με carfilzomib και δεξαμεθαζόνη σημαίνει ότι οι ασθενείς που ζουν με πολλαπλούν μυέλωμα στην Ευρώπη μπορούν πλέον να λαμβάνουν isatuximab σε συνδυασμό με δύο πρότυπα θεραπευτικών θεραπειών. Ο συνδυασμός carfilzomib και δεξαμεθαζόνης αντιπροσωπεύει ένα σημαντικό επίπεδο φροντίδας στην Ευρώπη. Η διαπίστωση της δοκιμής Φάσης 3 IKEMA ότι η προσθήκη του isatuximab σε αυτό το σχήμα μείωσε τον κίνδυνο εξέλιξης ή θανάτου σχεδόν κατά το ήμισυ αποτέλεσε τη βάση για αυτήν τη σημαντική έγκριση της Ευρωπαϊκής Επιτροπής."
Πηγές:
pharmaceutical-business-review.
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
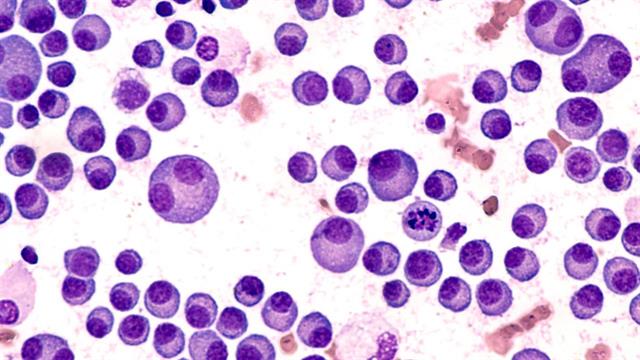
 Καθηγητής Δημόπουλος - Πολλαπλό μυέλωμα: Νέες θεραπείες αλλάζουν ριζικά την πρόγνωση της νόσου
Καθηγητής Δημόπουλος - Πολλαπλό μυέλωμα: Νέες θεραπείες αλλάζουν ριζικά την πρόγνωση της νόσου Θετικά στοιχεία από δοκιμή τελικού σταδίου για φάρμακο κατά του καρκίνου στο αίμα
Θετικά στοιχεία από δοκιμή τελικού σταδίου για φάρμακο κατά του καρκίνου στο αίμα "Κόκκινο" στο πολλαπλό μυέλωμα: "Ελπίζουμε πως σύντομα θα μιλάμε για ίαση"
"Κόκκινο" στο πολλαπλό μυέλωμα: "Ελπίζουμε πως σύντομα θα μιλάμε για ίαση" ΕΚΠΑ: Πού "τρέχουν" κλινικές μελέτες για το πολλαπλό μυέλωμα - Μάρτιος, μήνας ευαισθητοποίησης
ΕΚΠΑ: Πού "τρέχουν" κλινικές μελέτες για το πολλαπλό μυέλωμα - Μάρτιος, μήνας ευαισθητοποίησης Πολλαπλό μυέλωμα: Νέα γενιά φαρμάκων δημιουργεί ελπίδες
Πολλαπλό μυέλωμα: Νέα γενιά φαρμάκων δημιουργεί ελπίδες Ελπίδα για ασθενείς με υποτροπιάζον - ανθεκτικό πολλαπλούν μυέλωμα [μελέτη]
Ελπίδα για ασθενείς με υποτροπιάζον - ανθεκτικό πολλαπλούν μυέλωμα [μελέτη] Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς