Ο FDA ενέκρινε το πρώτο χάπι για την αντιμετώπιση ενηλίκων με σοβαρή αλωπεκία.
Το baricitinib είναι η πρώτη θεραπεία για τη γυροειδή αλωπεκία που εγκρίθηκε από τον Οργανισμό, η οποία αντιμετωπίζει όλο το σώμα παρά ένα συγκεκριμένο σημείο.
Το Olumiant ανήκει στους Jak Inhibitors και δρα παρεμβαλλόμενο με την κυτταρική οδό που προκαλεί φλεγμονή. Εγκρίθηκε πρώτη φορά το 2018 για τη ρευματοειδή αρθρίτιδα.
Το φάρμακο της Eli Lilly βασίζεται σε 2 κλινικές δοκιμές που περιέλαβαν 1.200 ασθενείς με αλωπεκία με τουλάχιστον 50% απώλεια μαλλιών, που έλαβαν είτε 2 είτε 4 mg Olumiant ή placebo καθημερινά.
Μετά από 36 εβδομάδες, τα ποσοστά ασθενών που πέτυχαν τουλάχιστον 80% κάλυψη μαλλιών ήταν 17% και 22% για αυτούς που έλαβαν 2 mg Olumiant και 32% και 35% για όσους έλαβαν 4 mg του φαρμάκου.
Αυτό, σε σύγκριση με 3% και 5% όσων έλαβαν placebo.
Στις πιο συχνές ανεπιθύμητες ενέργειες περιλαμβάνονταν: Λοιμώξεις του ανώτερου αναπνευστικού, πονοκέφαλος, ακμή, υψηλή χοληστερόλη, λοιμώξεις ουροποιητικού, αύξηση ηπατικών ενζύμων, φλεγμονή των υλάκων, κόπωση, λοιμώξεις του κατώτερου αναπνευστικού, ναυτία, αναιμία, πόνος στην κοιλιά, αύξηση βάρους, χαμηλά επίπεδα ορισμένων τύπων λευκών αιμοσφαιρίων.
Το Olumiant δεν θα πρέπει να χρησιμοποιείται σε συνδυασμό με άλλους JAK inhibitors ή άλλα ισχυρά ανοσοκατασταλτικά. Το φάρμακο φέρει προειδοποίηση στη συσκευασία για σοβαρές λοιμώξεις, θάνατο, καρκίνο, καρδιακά προβλήματα και θρόμβους.
Ο FDA συμβουλεύει ότι οι ασθενείς που λαμβάνουν το φάρμακο θα πρέπει να παρακολουθούνται στενά για λοίμωξη πριν και μετά την αγωγή και θα πρέπει να ελεγχθούν για λανθάνουσα και ενεργή φυματίωση πριν την αγωγή.
Προσθέστε το iatronet.gr στο DiscoverΕιδήσεις υγείας σήμερα
Πολλαπλάσια κρούσματα νόσου λεγεωνάριων στην Ελλάδα την τελευταία εξαετία [πίνακας]
ΕΟΔΥ: Χαμηλή διασπορά γρίπης, κορωνοϊού - Ένας θάνατος ασθενή με CoViD - Σε ύφεση και ο RSV
Sidevit® B12: Νέα εποχή στην απορρόφηση της βιταμίνης Β12

 Γυροειδής αλωπεκία: Νέα κατευθυντήρια γραμμή για διάγνωση και θεραπεία
Γυροειδής αλωπεκία: Νέα κατευθυντήρια γραμμή για διάγνωση και θεραπεία Γυροειδής αλωπεκία: Σχετίζεται με φλεγμονώδεις νόσους;
Γυροειδής αλωπεκία: Σχετίζεται με φλεγμονώδεις νόσους;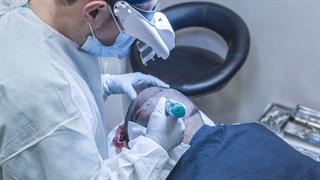 Μεταμόσχευση Μαλλιών: Σύγχρονες Έννοιες και Τεχνικές
Μεταμόσχευση Μαλλιών: Σύγχρονες Έννοιες και Τεχνικές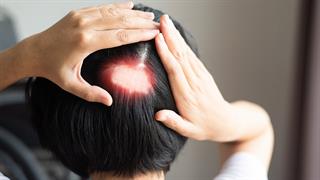 Η γυροειδής αλωπεκία συνδέεται με μεγαλύτερη εμφάνιση αυτοάνοσων και παθήσεων ψυχικής υγείας [μελέτη]
Η γυροειδής αλωπεκία συνδέεται με μεγαλύτερη εμφάνιση αυτοάνοσων και παθήσεων ψυχικής υγείας [μελέτη] Συσχέτιση αυτοάνοσων νοσημάτων, όπως της γυροειδούς αλωπεκίας, με τη νόσηση από COVID-19
Συσχέτιση αυτοάνοσων νοσημάτων, όπως της γυροειδούς αλωπεκίας, με τη νόσηση από COVID-19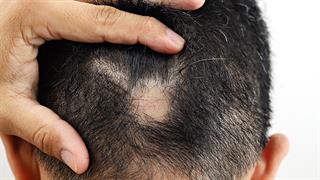 Αναστολείς JAK αντιμετωπίζουν αποτελεσματικά τη γυροειδή αλωπεκία [μελέτη]
Αναστολείς JAK αντιμετωπίζουν αποτελεσματικά τη γυροειδή αλωπεκία [μελέτη] Πολλαπλάσια κρούσματα νόσου λεγεωνάριων στην Ελλάδα την τελευταία εξαετία [πίνακας]
Πολλαπλάσια κρούσματα νόσου λεγεωνάριων στην Ελλάδα την τελευταία εξαετία [πίνακας] "Αττικόν" - Διοίκηση για κρούσματα γαστρεντερίτιδας από νοροϊό: Το νοσοκομείο λειτουργεί κανονικά
"Αττικόν" - Διοίκηση για κρούσματα γαστρεντερίτιδας από νοροϊό: Το νοσοκομείο λειτουργεί κανονικά 'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι
'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι Το junk food στην παιδική ηλικία διαταράσσει περιοχές του εγκεφάλου
Το junk food στην παιδική ηλικία διαταράσσει περιοχές του εγκεφάλου 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Nέες αποχωρήσεις στελεχών
Nέες αποχωρήσεις στελεχών Τι είναι η ALS από την οποία πέθανε ο Παρασκευάς Άντζας στα 49 του
Τι είναι η ALS από την οποία πέθανε ο Παρασκευάς Άντζας στα 49 του Φρούτα με την περισσότερη και λιγότερη φρουκτόζη
Φρούτα με την περισσότερη και λιγότερη φρουκτόζη 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά