Παρά τη μεγάλη επιτυχία της θεραπείας με CAR-T κύτταρα σε επιθετικά λεμφώματα Β-κυττάρων, περίπου το 60% των ασθενών δεν παρουσιάζει μόνιμη ύφεση. Σε αυτούς τους ασθενείς, ο συνδυασμός με έναν αναστολέα CSF1R θα μπορούσε να βελτιώσει την αποτελεσματικότητα.
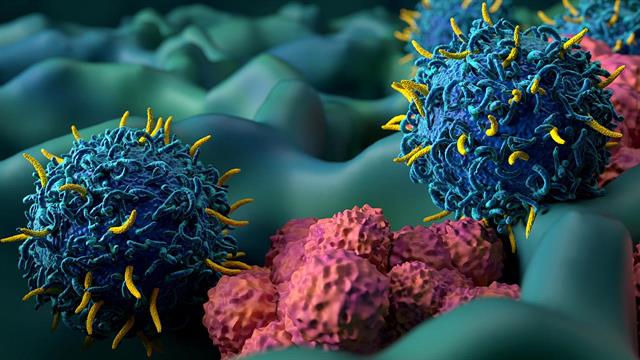
Τα CAR-T κύτταρα εντοπίζουν καρκινικά κύτταρα με συγκεκριμένα χαρακτηριστικά επιφάνειας και τα εξοντώνουν. Ωστόσο, σε ορισμένους ασθενείς αυτό δεν λειτουργεί μακροπρόθεσμα.
Η χρήση Τ-κυττάρων με χιμαιρικό υποδοχέα αντιγόνου (CAR-T-κυτταρική θεραπεία) έχει φέρει επανάσταση στη θεραπεία ασθενών με υποτροπιάζον ή ανθεκτικό (r/r) επιθετικό λέμφωμα Β-κυττάρων (B-NHL).
Ωστόσο, έως και τα δύο τρίτα των ασθενών με B-NHL που έλαβαν θεραπεία με κύτταρα CAR-T αντι-CD19 δεν παρουσιάζουν μακροπρόθεσμα οφέλη.
Πολλές αιτίες για αυτή την ανεπαρκή ανταπόκριση έχουν συζητηθεί, μεταξύ των οποίων η υπορύθμιση ή η μετάλλαξη του CD19, η επέκταση των ρυθμιστικών CAR-T κυττάρων (CAR-Treg κύτταρα) και ένα κατασταλτικό μικροπεριβάλλον όγκου λεμφώματος (TME).
Το πρόβλημα του TME εξετάζεται τώρα από μια ομάδα με επικεφαλής την Δρ. David Stahl από το Πανεπιστήμιο της Κολωνίας, η οποία δημοσίευσε τα ευρήματά της στο επιστημονικό περιοδικό "Cancer Cell".
Η ομάδα των συγγραφέων διαπίστωσε ότι σε ασθενείς που δεν ανταποκρίθηκαν μόνιμα στη θεραπεία με κύτταρα CAR-T αντι-CD-19, πριν από τη θεραπεία υπήρχε σημαντική συγκέντρωση ενός συγκεκριμένου πληθυσμού κυττάρων.
Αυτά τα λεγόμενα LAMM κύτταρα (λεμφοειδή μονοκυτταρικά κύτταρα που σχετίζονται με λέμφωμα) εξέφραζαν τον υποδοχέα του παράγοντα 1 που διεγείρει την αποικία (CSF1R) καθώς και τους επιφανειακούς δείκτες CD14 και CD68 (CSF1R+CD14+CD68+).
Τόσο σε δείγματα ασθενών όσο και σε ένα μοντέλο ποντικού για διάχυτο μεγάλο κυτταρικό λέμφωμα Β, αποδείχθηκε ότι τα κύτταρα LAMM διαφοροποιούνται μέσω της οδού σηματοδότησης CSF1R-PI3K/AKT/mTOR.
Αυτή η οδός σηματοδότησης που ενεργοποιείται από τον υποδοχέα CSF1R παίζει καθοριστικό ρόλο στη διαφοροποίηση, τον πολλαπλασιασμό, τη λειτουργία και την επιβίωση των κυττάρων του μυελοειδούς συστήματος, ιδίως των μονοκυττάρων και των μακροφάγων. Σε ογκολογικό πλαίσιο, αυτή η οδός μπορεί να προάγει ανοσοκατασταλτικές κυτταρικές λειτουργίες, ιδίως στο TME.
Ex vivo, τα ανθρώπινα κύτταρα LAMM ήταν ικανά να καταστείλουν σημαντικά τον πολλαπλασιασμό και την κυτταροτοξικότητα των αντι-CD19 CAR-T κυττάρων.
Οι ερευνητές μπόρεσαν να δείξουν ότι η ανοσοκαταστολή ξεπερνιέται όταν αναστέλλεται το CSF1R.
Στο μοντέλο ποντικιών, ο συνδυασμός αναστολής CSF1R και CAR-T-κυττάρων οδήγησε σε δραστική βελτίωση της επέκτασης των CAR-T-κυττάρων στον σπλήνα, σε μείωση της διήθησης των LAMM-κυττάρων, σε αυξημένη διήθηση CD8+-Τ-κυττάρων, σε αναδιάρθρωση του TME σε ένα πλούσιο σε Τ-κύτταρα, φολικουλική αρχιτεκτονική και στην ομαλοποίηση του αγγειακού συστήματος του όγκου.
Τελικά, η αναστολή του CSF1R οδήγησε σε σημαντικά παρατεταμένη επιβίωση χωρίς εξέλιξη της νόσου και συνολική επιβίωση, με ταυτόχρονη μείωση της έκφρασης κυτοκινών που σχετίζονται με σύνδρομο απελευθέρωσης κυτοκινών ή σύνδρομο νευροτοξικότητας που σχετίζεται με κύτταρα του ανοσοποιητικού συστήματος.
Δεδομένου ότι οι αναστολείς CSF1R (π.χ. πεξιδαρτινίμπη) έχουν ήδη εγκριθεί για άλλες ενδείξεις, τουλάχιστον στις ΗΠΑ, τα δεδομένα αυτά παρέχουν μια λογική βάση για την κλινική αξιολόγηση της συνδυαστικής θεραπείας με κύτταρα CAR-T αντι-CD19 και αναστολή CSF1R σε ασθενείς με r/r B-NHL.
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
 Νέα ανακάλυψη για το Alzheimer: Σημαντικό εύρημα συνδέεται με την εξέλιξη της νόσου
Νέα ανακάλυψη για το Alzheimer: Σημαντικό εύρημα συνδέεται με την εξέλιξη της νόσου Ξένα κύτταρα μέσα μας: Οι επιστήμονες ερευνούν το φαινόμενο του μικροχιμαιρισμού
Ξένα κύτταρα μέσα μας: Οι επιστήμονες ερευνούν το φαινόμενο του μικροχιμαιρισμού Αντικαρκινικό φάρμακο αντιμετωπίζει τις γενετικές βλάβες στα κακοήθη κύτταρα
Αντικαρκινικό φάρμακο αντιμετωπίζει τις γενετικές βλάβες στα κακοήθη κύτταρα Πώς τα ανθρώπινα κύτταρα αναγνωρίζουν την υπονόμευση της άμυνάς τους από ιούς
Πώς τα ανθρώπινα κύτταρα αναγνωρίζουν την υπονόμευση της άμυνάς τους από ιούς Πώς ο κυτταρικός μεταβολισμός ρυθμίζει τη γήρανση της καρδιάς
Πώς ο κυτταρικός μεταβολισμός ρυθμίζει τη γήρανση της καρδιάς Η καρδιά αναγεννά μυϊκά κύτταρα μετά από καρδιακή προσβολή [μελέτη]
Η καρδιά αναγεννά μυϊκά κύτταρα μετά από καρδιακή προσβολή [μελέτη] Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς