Η Janssen Pharmaceutical, μέλος της Johnson & Johnson, εξασφάλισε την έγκριση από την Ευρωπαϊκή Επιτροπή (EC) για εκτεταμένη χρήση του ibrutinib σε συνδυασμό με το rituximab για ενήλικες ασθενείς που δεν είχαν λάβει προηγουμένως θεραπεία για χρόνια λεμφοκυτταρική λευχαιμία (CLL).
Η διευρυμένη έγκριση βασίστηκε σε δεδομένα της μελέτης φάσης 3 E1912, η οποία έδειξε ότι οι ασθενείς που δεν είχαν λάβει προηγούμενη θεραπεία, ηλικίας 70 ετών ή και νεότεροι που έλαβαν θεραπεία με ibrutinib και rituximab έζησαν περισσότερο χωρίς πρόοδο της νόσου από αυτούς που έλαβαν θεραπεία με το καθιερωμένο σχήμα χημειο-ανοσοθεραπείας φλουδαραβίνη, κυκλοφωσφαμίδη και ριτουξιμάμπη ( FCR).
Η Ομάδα Έρευνας για τον Καρκίνο ECOG-ACRIN (ECOG-ACRIN) σχεδίασε και πραγματοποίησε τη μελέτη στις ΗΠΑ. Χρηματοδοτήθηκε από το Εθνικό Ινστιτούτο Καρκίνου (NCI), το οποίο είναι μέρος των Εθνικών Ινστιτούτων Υγείας των ΗΠΑ.
Τον Απρίλιο του τρέχοντος έτους, η εταιρεία εξασφάλισε έγκριση από την Αμερικανική Υπηρεσία Τροφίμων και Φαρμάκων για το Imbruvica και rituximab για την ίδια ένδειξη.
Ο αντιπρόεδρος της Janssen Research & Development στο τμήμα της ογκολογίας και της κλινικής ανάπτυξης Dr Craig Tendler, δήλωσε:
"Αυτό το τελευταίο ορόσημο υπογραμμίζει τη δέσμευσή μας να μελετήσουμε το πλήρες δυναμικό του ibrutinib αναπτύσσοντας θεραπείες που μπορούν να καταπολεμήσουν την χρόνια λεμφοκυτταρική λευχαιμία (CLL).
Πηγές:
pharmaceutical business review
Ειδήσεις υγείας σήμερα
11η εκστρατεία της ΑΜΚΕ Με Οδηγό το Διαβήτη: 25 αδιάγνωστα περιστατικά διαβήτη και νεφρικής νόσου και δεκάδες αρρύθμιστοι διαβητικοί
Διαβήτης: Οι λοιμώξεις αποτελούν σημαντικό κίνδυνο [μελέτη]
Η γυναικεία γονιμότητα μπορεί να βλάπτεται από τη χρόνια στοματική φλεγμονή
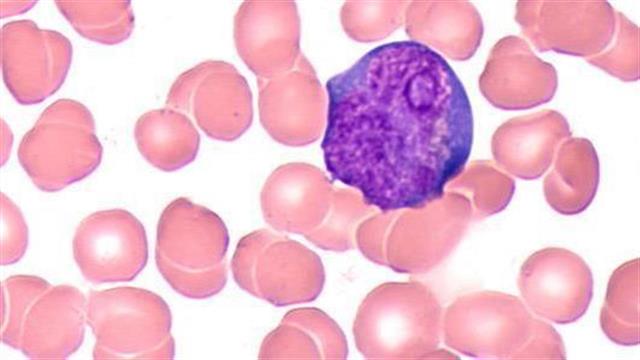
 Ελπίδες για τη θεραπεία της οξείας μυελογενούς λευχαιμίας στα παιδιά
Ελπίδες για τη θεραπεία της οξείας μυελογενούς λευχαιμίας στα παιδιά Ο Χοσέ Καρέρας συγκέντρωσε 3,4 εκατομμύρια ευρώ για το Ίδρυμα λευχαιμίας
Ο Χοσέ Καρέρας συγκέντρωσε 3,4 εκατομμύρια ευρώ για το Ίδρυμα λευχαιμίας Μηχανισμός κυτταρικής προστασίας προστατεύει από την οξεία μυελογενή λευχαιμία
Μηχανισμός κυτταρικής προστασίας προστατεύει από την οξεία μυελογενή λευχαιμία siREN: Χρυσό μετάλλιο στη θεραπευτική πρόταση του ΑΠΘ για τη χρόνια λεμφοκυτταρική λευχαιμία
siREN: Χρυσό μετάλλιο στη θεραπευτική πρόταση του ΑΠΘ για τη χρόνια λεμφοκυτταρική λευχαιμία Ελπίδες για τα παιδιά με λευχαιμία: Μέχρι και 90% πιθανότητες ίασης
Ελπίδες για τα παιδιά με λευχαιμία: Μέχρι και 90% πιθανότητες ίασης Λευχαιμία στα παιδιά - Καλύτερη θεραπεία με την τεχνητή νοημοσύνη
Λευχαιμία στα παιδιά - Καλύτερη θεραπεία με την τεχνητή νοημοσύνη Βραδινές συνήθειες για πιο υγιές έντερο
Βραδινές συνήθειες για πιο υγιές έντερο Γενικό Νοσοκομείο Κατερίνης: Eγκαίνια της νέας Παθολογικής Κλινικής συνολικού ύψους 650.000 ευρώ
Γενικό Νοσοκομείο Κατερίνης: Eγκαίνια της νέας Παθολογικής Κλινικής συνολικού ύψους 650.000 ευρώ Διαβήτης: Οι λοιμώξεις αποτελούν σημαντικό κίνδυνο [μελέτη]
Διαβήτης: Οι λοιμώξεις αποτελούν σημαντικό κίνδυνο [μελέτη] Νέα ελπίδα για το Πάρκινσον: Η δραστική ουσία που ανοίγει νέους δρόμους θεραπείας
Νέα ελπίδα για το Πάρκινσον: Η δραστική ουσία που ανοίγει νέους δρόμους θεραπείας Ι. Καβαλιώτης: Αποχαιρετισμός σε έναν δάσκαλο των παιδιατρικών λοιμώξεων
Ι. Καβαλιώτης: Αποχαιρετισμός σε έναν δάσκαλο των παιδιατρικών λοιμώξεων 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] 'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι
'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι Ozempic effect στην κατανάλωση του σούπερ μάρκετ
Ozempic effect στην κατανάλωση του σούπερ μάρκετ Μαλώνοντας σε ξένο... ΗΤΑρώνα - Τι αλλάζει στη διαδικασία αξιολόγησης φαρμάκων
Μαλώνοντας σε ξένο... ΗΤΑρώνα - Τι αλλάζει στη διαδικασία αξιολόγησης φαρμάκων Μ. Σύρρου: Ο ολοκληρωμένος γενωμικός νεογνικός έλεγχος απαιτεί σαφές θεσμικό πλαίσιο λειτουργίας
Μ. Σύρρου: Ο ολοκληρωμένος γενωμικός νεογνικός έλεγχος απαιτεί σαφές θεσμικό πλαίσιο λειτουργίας Ξεκινώντας από την "κούνια" - Βρέφη, οθόνες και αναπτυξιακά ελλείμματα
Ξεκινώντας από την "κούνια" - Βρέφη, οθόνες και αναπτυξιακά ελλείμματα