Η Mylan και ο εταίρος Biocon έλαβαν ευρωπαϊκή έγκριση για βιοομοειδές προϊόν ινσουλίνης.
Η ρυθμιστική αρχή φαρμάκων της Αυστραλίας, η Therapeutic Goods Administration (TGA), έδωσε επίσης στη θεραπεία το πράσινο φως.
Πρόκειται για προγεμισμένο στυλό μιας χρήσης για άτομα με διαβήτη και είναι το πρώτο βιοομοειδές από το κοινό χαρτοφυλάκιο της Biocon και της Mylan που θα εγκριθεί στην Ευρώπη.
Οι επιχειρήσεις έχουν μακρόχρονη συνεργασία, η οποία ξεκίνησε το 2013, όταν η Actavis αποχώρησε από την επιχείρηση για την ανάπτυξη βιοομοειδών προϊόντων ινσουλίνης.
Ο διαβήτης είναι η ταχύτερα αναπτυσσόμενη αγορά της φαρμακευτικής βιομηχανίας, με τους ερευνητές να εκτιμούν ότι μέχρι το 2030, το παγκόσμιο κόστος πρόληψης και θεραπείας θα μπορούσε να φτάσει σχεδόν το μισό τρισεκατομμύριο δολάρια.
Ο πρόεδρος της Mylan, Rajiv Malik, δήλωσε: "Οι επενδύσεις που πραγματοποιήσαμε για να αναπτύξουμε και να κατασκευάσουμε ένα κορυφαίο χαρτοφυλάκιο πολύπλοκων προϊόντων, συμπεριλαμβανομένου του βιοομοειδούς ινσουλίνης, είναι ένας τρόπος να υλοποιήσουμε τη δέσμευσή μας να επεκτείνουμε την πρόσβαση σε υψηλής ποιότητας ιατρική".
Ειδήσεις υγείας σήμερα
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Πώς θα προλάβουμε τον διαβήτη
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε

 Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη
Άνοιξε η πόρτα για αποζημίωση των CGM σε άτομα με διαβήτη τύπου 2 που λαμβάνουν ινσουλίνη Φαρμασέρβ - Λίλλυ: Δεν επηρεάζεται η διάθεση ινσουλινών της εταιρείας στην Ελλάδα
Φαρμασέρβ - Λίλλυ: Δεν επηρεάζεται η διάθεση ινσουλινών της εταιρείας στην Ελλάδα Πειραματικό χάπι ινσουλίνης μειώνει το σάκχαρο σε πειραματόζωα
Πειραματικό χάπι ινσουλίνης μειώνει το σάκχαρο σε πειραματόζωα Εμμηνόπαυση: Τα επίπεδα ινσουλίνης συνδέονται με εξάψεις και νυχτερινές εφιδρώσεις [μελέτη]
Εμμηνόπαυση: Τα επίπεδα ινσουλίνης συνδέονται με εξάψεις και νυχτερινές εφιδρώσεις [μελέτη]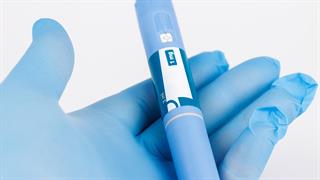 Εβδομαδιαίες ινσουλίνες - Τι προσφέρουν στον ασθενή
Εβδομαδιαίες ινσουλίνες - Τι προσφέρουν στον ασθενή Η μάχη της ινσουλίνης στην άλλη πλευρά του Ατλαντικού
Η μάχη της ινσουλίνης στην άλλη πλευρά του Ατλαντικού Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε
Χρόνια νεφρική νόσος: Τι πρέπει να γνωρίζουμε Πώς θα προλάβουμε τον διαβήτη
Πώς θα προλάβουμε τον διαβήτη Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε
Αλκοόλ και αντικαταθλιπτικά: Γιατί δεν πρέπει να τα συνδυάζουμε Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε
Μικροβιακή αντοχή: Μία πανδημία σε αργή κίνηση που μπορούμε να αποτρέψουμε 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic]
Προβλήματα πρόσβασης σε θεραπεία αποσιδήρωσης [infographic] Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ
Κεραμέως: Βαρέα και ανθυγιεινά για νοσηλευτές και διασώστες ΕΚΑΒ Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς