O Οργανισμός Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ ενέκρινε το υποδόρια ενέσιμο Dupilumab, τον πρώτο και μοναδικό βιολογικό παράγοντα που λαμβάνει έγκριση για τη θεραπεία ενηλίκων με μέτρια έως σοβαρή ατοπική δερματίτιδα των οποίων η νόσος δεν ελέγχεται επαρκώς με συνταγογραφούμενες θεραπείες που εφαρμόζονται τοπικά ή στην περίπτωση που οι συγκεκριμένες θεραπείες δεν ενδείκνυνται. Αυτό ανακοίνωσαν η Sanofi και η Regeneron Pharmaceuticals, Inc.
“Τα άτομα με μέτρια έως σοβαρή ατοπική δερματίτιδα αντιμετωπίζουν έντονα, συχνά αφόρητα συμπτώματα που ενδέχεται να τους επηρεάζουν για το μεγαλύτερο μέρος της ζωής τους,” δήλωσε η Julie Block, Πρόεδρος και CEO της National Eczema Association (Εθνική Ένωση για το Έκζεμα των ΗΠΑ). “Μέχρι σήμερα, υπήρχαν λίγες διαθέσιμες επιλογές για τη θεραπεία των ατόμων με μη ελεγχόμενη μέτρια έως σοβαρή ατοπική δερματίτιδα. Για αυτό το λόγο η σημερινή έγκριση του Dupilumab είναι ιδιαίτερα σημαντική για την κοινότητά μας. Έχουμε πλέον στη διάθεσή μας μια θεραπεία που αναμένεται να βοηθήσει τους ασθενείς που πάσχουν από αυτή την εξουθενωτική ασθένεια.”
Το Dupilumab είναι ένα ανθρώπινο μονοκλωνικό αντίσωμα το οποίο έχει σχεδιαστεί για να αναστέλλει ειδικά την υπερενεργή σηματοδότηση δύο βασικών κυτοκινών, της IL-4 και της IL-13, που πιστεύεται ότι αποτελούν σημαντικό παράγοντα της επίμονης υποκείμενης φλεγμονής στην ατοπική δερματίτιδα. Το Dupilumab παρέχεται σε προγεμισμένη σύριγγα και μπορεί να χορηγηθεί από τον ίδιο τον ασθενή υποδόρια κάθε δεύτερη εβδομάδα μετά την αρχική δόση φόρτισης. Το Dupilumab μπορεί να χρησιμοποιείται με ή χωρίς τοπικά κορτικοστεροειδή. Δεν θα πρέπει να χορηγείται σε ασθενείς που είναι αλλεργικοί στο Dupilumab ή σε κάποιο άλλο από τα συστατικά του φαρμακευτικού σκευάσματος.
Η ατοπική δερματίτιδα, η πιο συνηθισμένη μορφή εκζέματος, αποτελεί μία χρόνια φλεγμονώδη νόσο με συμπτώματα που συχνά παρουσιάζονται ως εξάνθημα στην επιφάνεια του δέρματος. Η μέτρια έως σοβαρή ΑΔ χαρακτηρίζεται από εξανθήματα, που συχνά καλύπτουν μεγάλο τμήμα του σώματος, και είναι δυνατό να συνοδεύεται από έντονο, συνεχή κνησμό, ξηρότητα, σκάσιμο, ερυθρότητα, δημιουργία εφελκίδων και εξιδρώματος. Ο κνησμός είναι ένα από τα πιο δύσκολα συμπτώματα των ασθενών που ενδέχεται να καταστεί εξουθενωτικός. Υπολογίζεται ότι 300.000 από τους ενήλικες με μη ελεγχόμενη μέτρια έως σοβαρή ατοπική δερματίτιδα στις ΗΠΑ έχουν τη μεγαλύτερη ανάγκη για νέες θεραπευτικές επιλογές.
“Το Dupilumab είναι το αποτέλεσμα ετών έρευνας σχετικά με τα υποκείμενα αίτια αλλεργικών και ατοπικών νόσων από τους επιστήμονές μας. Στην ατοπική δερματίτιδα, το Dupilumab έδειξε ότι συμβάλλει στην υποχώρηση των δερματικών βλαβών και τη διαχείριση του έντονου κνησμού που προκαλείται από τη νόσο,” δήλωσε ο George D. Yancopoulos, M.D., Ph.D., Founding Scientist, President και Chief Scientific Officer της Regeneron. “Η σημερινή έγκριση δεν θα ήταν δυνατή χωρίς την αφοσίωση των κλινικών ερευνητών και τη συμμετοχή των ασθενών στο παγκόσμιο κλινικό πρόγραμμα LIBERTY AD.”
Το Dupilumab αξιολογήθηκε από τον Οργανισμό Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ μέσω της διαδικασίας Ταχείας Αξιολόγησης, η οποία ακολουθείται για φάρμακα με δυνητικά σημαντικά βελτιωμένη ασφάλεια ή αποτελεσματικότητα κατά τη θεραπεία σοβαρών παθήσεων.
Είχε προηγηθεί ο χαρακτηρισμός του Duxipent ως Σημαντικής Καινοτόμου Θεραπείας (Breakthrough Therapy) για την ανεπαρκώς ελεγχόμενη μέτρια έως σοβαρή ατοπική δερματίτιδα από τον FDA το 2014. Ο χαρακτηρισμός Σημαντική Καινοτόμα Θεραπεία (Breakthrough Therapy) δημιουργήθηκε από τον FDA για να επισπεύσει την ανάπτυξη και αξιολόγηση φαρμάκων που αναπτύσσονται για σοβαρές ή απειλητικές για τη ζωή παθήσεις. Το Dupilumab αποτελεί την πρώτη περίπτωση φαρμάκου που του αποδόθηκε αυτός ο χαρακτηρισμός για δερματολογική νόσο πλην των δερματολογικών καρκίνων.
“Επιδιώκουμε να μετατρέψουμε την επιστημονική καινοτομία σε θεραπευτικές λύσεις που επιφέρουν ουσιαστικές αλλαγές στη ζωή των ανθρώπων,” δήλωσε ο Olivier Brandicourt, M.D., Chief Executive Officer της Sanofi. “Η έγκριση του Dupilumab δίνει νέα ελπίδα στους ενήλικες με μέτρια έως σοβαρή Ατοπική Δερματίτιδα στις ΗΠΑ και ανυπομονούμε να συνεργαστούμε με ρυθμιστικές αρχές ανά τον κόσμο προκειμένου να προσφέρουμε αυτό το σημαντικό νέο φάρμακο στους ασθενείς παγκοσμίως.”
Η Sanofi Genzyme, η παγκόσμια επιχειρησιακή μονάδα ειδικής θεραπείας της Sanofi, και η Regeneron είναι υπεύθυνες για την εμπορική κυκλοφορία του Dupilumab στις Ηνωμένες Πολιτείες. Το Dupilumab αναμένεται να είναι διαθέσιμο σε ασθενείς και προμηθευτές εντός της εβδομάδας στις ΗΠΑ.
Τον Δεκέμβριο του 2016, ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) αποδέχτηκε προς εξέταση την Αίτηση Άδειας Κυκλοφορίας (MAA) της Sanofi και της Regeneron για το Dupilumab για τη θεραπεία ενηλίκων με μη ελεγχόμενη μέτρια έως σοβαρή ατοπική δερματίτιδα.
Το Κλινικό Πρόγραμμα LIBERTY AD και τα Αποτελέσματά του
Η έγκριση του Dupilumab βασίστηκε σε στοιχεία από το παγκόσμιο κλινικό πρόγραμμα LIBERTY AD, το οποίο περιλαμβάνει τρεις τυχαιοποιημένες Φάσης 3 πιλοτικές κλινικές μελέτες γνωστές ως SOLO 1, SOLO 2 και CHRONOS (με τη συμμετοχή συνολικά 2.119 ενηλίκων ασθενών). Οι μελέτες αξιολόγησαν τη χρήση του Dupilumab είτε ως μονοθεραπείας (μελέτες SOLO 1 ή SOLO 2, στις οποίες συμμετείχαν 1.379 ενήλικες ασθενείς) είτε ως ταυτόχρονης χορήγησης με τοπικά κορτικοστεροειδή (μελέτη CHRONOS, στην οποία συμμετείχαν 740 ενήλικες ασθενείς) σε ασθενείς με ανεπαρκώς ελεγχόμενη μέτρια έως σοβαρή ΑΔ. Σε όλες αυτές τις μελέτες, το Dupilumab ως μονοθεραπεία ή σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχε τα πρωτεύοντα και κύρια δευτερεύοντα καταληκτικά σημεία, και πιο συγκεκριμένα:
Στις μελέτες SOLO 1 και SOLO 2, η μονοθεραπεία με Dupilumab βελτίωσε σημαντικά παραμέτρους που σχετίζονταν με την υποχώρηση των δερματικών βλαβών και τη συνολική έκταση και σοβαρότητα της νόσου:
- Τη 16η εβδομάδα, στις μελέτες SOLO 1 και SOLO 2, αντίστοιχα, το 38% και το 36% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες πέτυχαν πλήρη ή σχεδόν πλήρη υποχώρηση των δερματικών βλαβών με βάση την 5-βάθμια κλίμακα IGA (Investigator's Global Assessment/Συνολική Αξιολόγηση του Ερευνητή) (πρωτεύον καταληκτικό σημείο), σε σύγκριση με το 10% και 9% των ασθενών που έλαβαν εικονικό φάρμακο.
- Τη 16η εβδομάδα, στις μελέτες SOLO 1 and SOLO 2, αντίστοιχα, το 51 και 44% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες πέτυχαν μείωση κατά 75% ή υψηλότερη βάσει του δείκτη EASI-75 (Eczema Area and Severity Index/Δείκτης Έκτασης και Βαρύτητας του Εκζέματος) από την έναρξη της μελέτης, ένα κύριο δευτερεύον καταληκτικό σημείο, σε σύγκριση με το 15% και το 12% των ασθενών που έλαβαν εικονικό φάρμακο.
- Τη 16η εβδομάδα, στις μελέτες SOLO 1 and SOLO 2, αντίστοιχα, το 41% και το 36% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες πέτυχαν βελτίωση τεσσάρων μονάδων ή υψηλότερη της καθημερινής έντασης του αναφερόμενου από τον ασθενή κνησμού, με βάση την αριθμητική κλίμακα (NRS) (Pruritus Numerical Rating Scale/αριθμητική κλίμακα μέτρησης του κνησμού), σε σύγκριση με το 12% και το 10% των ασθενών που έλαβαν εικονικό φάρμακο.
Στη μελέτη CHRONOS, η θεραπεία με Dupilumab σε συνδυασμό με τοπικά κορτικοστεροειδή βελτίωσε σημαντικά παραμέτρους που σχετίζονταν με τη συνολική βαρύτητα της νόσου κατά τη 16η και την 52η εβδομάδα σε σύγκριση με θεραπεία με εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή:
- Τη 16η εβδομάδα, το 39% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν πλήρη υποχώρηση ή σχεδόν πλήρη υποχώρηση των δερματικών βλαβών (IGA 0 or 1), το πρωτεύον καταληκτικό σημείο, σε σύγκριση με το 12% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή.
- Τη 16η εβδομάδα, το 69% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν μείωση κατά 75% βάσει του δείκτη EASI, ενός δείκτη που μετρά τη βαρύτητα του εκζέματος (κύριο δευτερεύον καταληκτικό σημείο), σε σύγκριση με το 23% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή.
- Τη 16η εβδομάδα, το 59% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν βελτίωση τεσσάρων μονάδων ή υψηλότερη της καθημερινής έντασης του αναφερόμενου από τον ασθενή κνησμού, με βάση την αριθμητική κλίμακα (NRS) (Pruritus Numerical Rating Scale/αριθμητική κλίμακα μέτρησης του κνησμού), σε σύγκριση με το 20% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή.
- Η μελέτη πέτυχε επίσης πρόσθετα κύρια δευτερεύοντα καταληκτικά σημεία την 52η εβδομάδα, τα οποία έδειξαν ότι το 36% των ασθενών που έλαβαν Dupilumab 300 mg κάθε δύο εβδομάδες σε συνδυασμό με τοπικά κορτικοστεροειδή πέτυχαν πλήρη υποχώρηση ή σχεδόν πλήρη υποχώρηση των δερματικών βλαβών (IGA 0 or 1), σε σύγκριση με το 13% των ασθενών που έλαβαν εικονικό φάρμακο σε συνδυασμό με τοπικά κορτικοστεροειδή.
Οι πιο συχνά αναφερόμενες ανεπιθύμητες ενέργειες που παρατηρήθηκαν σε ποσοστό ίσο ή υψηλότερο του 1% κατά τη θεραπεία με Dupilumab είναι αντιδράσεις στο σημείο έγχυσης, φλεγμονή του οφθαλμού και του βλεφάρου, που περιλαμβάνει ερυθρότητα, οίδημα και κνησμός, καθώς και ψυχρά έλκη στο στόμα ή τα χείλη.
Επισκόπηση του Προγράμματος για το Dupilumab
Επί του παρόντος, το Dupilumab αξιολογείται στο πλαίσιο ενός ολοκληρωμένου προγράμματος ανάπτυξης για την Ατοπική Δερματίτιδα το οποίο περιλαμβάνει μελέτες σε παιδιά με σοβαρή Ατοπική Δερματίτιδα (ηλικίας 6 μηνών έως 11 ετών) και σε έφηβους με μέτρια έως σοβαρή Ατοπική Δερματίτιδα (ηλικίας 12 έως 17 ετών). Τον Οκτώβριο του 2016, ο Οργανισμός Τροφίμων και Φαρμάκων (FDA) των ΗΠΑ απέδωσε στο dupilumab τον χαρακτηρισμό Σημαντικής Καινοτόμου Θεραπείας (Breakthrough Therapy) και για τους δύο πληθυσμούς ασθενών. Οι δυνητικές αυτές χρήσεις βρίσκονται υπό δοκιμή και η ασφάλεια και αποτελεσματικότητά τους δεν έχουν αξιολογηθεί ή επιβεβαιωθεί από καμία ρυθμιστική αρχή.
Το Dupilumab αξιολογείται επίσης για άλλες φλεγμονώδεις νόσους για τις οποίες πιστεύεται ότι οι κυτοκίνες IL- 4 και IL-13 αποτελούν σημαντικό παράγοντα, μεταξύ των οποίων το επίμονο μη ελεγχόμενο άσθμα (Φάσης 3, αναμένονται αποτελέσματα εντός του έτους), η ρινική πολυποδίαση (Φάσης 3) και ηωσινοφιλική οισοφαγίτιδα (Φάσης 2). Οι δυνητικές αυτές χρήσεις βρίσκονται υπό δοκιμή και η ασφάλεια και αποτελεσματικότητά τους δεν έχουν αξιολογηθεί ή επιβεβαιωθεί από καμία ρυθμιστική αρχή.
Προσθέστε το iatronet.gr στο DiscoverΕιδήσεις υγείας σήμερα
Eμπορευματοποίηση της σύγχρονης Ιατρικής
Μπορώ να αυξήσω τη μυϊκή μου μάζα με γυμναστική στο σπίτι;
ΕΟΔΥ για την Ημέρα κατά του Καπνίσματος: Συμβουλευτική υποστήριξη μέσω της φωνητικής πύλης 1135

 Ατοπική δερματίτιδα και καλοκαίρι: Φίλος ή εχθρός ο ήλιος;
Ατοπική δερματίτιδα και καλοκαίρι: Φίλος ή εχθρός ο ήλιος;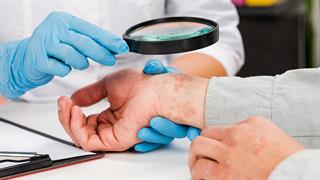 Το στρες συνδέεται με ατοπική δερματίτιδα
Το στρες συνδέεται με ατοπική δερματίτιδα Ατοπική δερματίτιδα: Ανακαλύφθηκε ο μηχανισμός του κνησμού
Ατοπική δερματίτιδα: Ανακαλύφθηκε ο μηχανισμός του κνησμού Ο FDA ενέκρινε κρέμα για την ατοπική δερματίτιδα στα παιδιά
Ο FDA ενέκρινε κρέμα για την ατοπική δερματίτιδα στα παιδιά Δείτε την Ατοπική Δερματίτιδα όπως πραγματικά είναι
Δείτε την Ατοπική Δερματίτιδα όπως πραγματικά είναι Ατοπική δερματίτιδα: Μπορεί ένα εμβόλιο να τη θεραπεύσει;
Ατοπική δερματίτιδα: Μπορεί ένα εμβόλιο να τη θεραπεύσει; Eμπορευματοποίηση της σύγχρονης Ιατρικής
Eμπορευματοποίηση της σύγχρονης Ιατρικής Μπορώ να αυξήσω τη μυϊκή μου μάζα με γυμναστική στο σπίτι;
Μπορώ να αυξήσω τη μυϊκή μου μάζα με γυμναστική στο σπίτι; Οικογενής υπερχοληστερολαιμία: Ελπίδες από γονιδιακή θεραπεία - Επιτυχής δοκιμή στη Βρετανία
Οικογενής υπερχοληστερολαιμία: Ελπίδες από γονιδιακή θεραπεία - Επιτυχής δοκιμή στη Βρετανία 31 Μαΐου: Παγκόσμια Ημέρα Κατά του Καπνίσματος - Καμπάνια ενημέρωσης από το ΕΛΙΚΑΡ
31 Μαΐου: Παγκόσμια Ημέρα Κατά του Καπνίσματος - Καμπάνια ενημέρωσης από το ΕΛΙΚΑΡ Nέες αποχωρήσεις στελεχών
Nέες αποχωρήσεις στελεχών Φρούτα με την περισσότερη και λιγότερη φρουκτόζη
Φρούτα με την περισσότερη και λιγότερη φρουκτόζη ΕΟΦ: Παράνομη διαφήμιση φαρμάκων για την παχυσαρκία - Τι να προσέχουν οι πολίτες
ΕΟΦ: Παράνομη διαφήμιση φαρμάκων για την παχυσαρκία - Τι να προσέχουν οι πολίτες 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] 'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι
'Εξαρση γαστρεντερίτιδας από νοροϊό στο "Αττικόν" - Τι καταγγέλλουν οι εργαζόμενοι Γεωργιάδης - νοσηλευτές: Προκήρυξη 3.694 θέσεων το 2026 και ένταξη στα Βαρέα
Γεωργιάδης - νοσηλευτές: Προκήρυξη 3.694 θέσεων το 2026 και ένταξη στα Βαρέα Κενό ασφάλειας στο σύστημα ιατρικών βεβαιώσεων - Τρίτοι είχαν πρόσβαση σε στοιχεία πολιτών
Κενό ασφάλειας στο σύστημα ιατρικών βεβαιώσεων - Τρίτοι είχαν πρόσβαση σε στοιχεία πολιτών