Για την πρώτη θεραπεία με μονοκλωνικά αντισώματα- lanadelumab- για την πρόληψη επαναλαμβανόμενων προσβολών από κληρονομικό αγγειοοίδημα (HAE) σε ασθενείς ηλικίας 12 ετών και άνω, συνιστά τη χορήγηση άδειας κυκλοφορίας ο Ευρωπαϊκός Οργανισμός Φαρμάκων.
Το HAE είναι μια μακροχρόνια εξασθενητική ασθένεια που χαρακτηρίζεται από προσβολές -οίδημα- κάτω από το δέρμα, ενώ μπορεί να συμβεί οπουδήποτε στο σώμα, όπως στο πρόσωπο, τα άκρα, το έντερο και τον λάρυγγα. Η ασθένεια αφορά ανωμαλίες που εμφανίζονται στο γονίδιο που είναι υπεύθυνο για την παραγωγή του αναστολέα C1 εστεράσης. Αυτό έχει ως αποτέλεσμα χαμηλά επίπεδα πρωτεΐνης C στο αίμα, γεγονός που συνεπάγεται αυξημένη δραστηριότητα της πρωτεΐνης καλλικρεϊνης και τελικά προκαλείται πρήξιμο. Όταν, όμως η διόγκωση συμβεί στο λάρυγγα, αυτό μπορεί να είναι απειλητικό για τη ζωή, καθώς μπορεί να φράξουν οι αεροφόροι οδοί εμποδίζοντας την αναπνοή.
Το lanadelumab είναι το πρώτο μονοκλωνικό αντίσωμα για την πρόληψη αυτής της νόσου. Έχει σχεδιαστεί για να αναγνωρίζει και να συνδέεται με τις πρωτεΐνες καλλικρεΐνης και έτσι να εμποδίζει τη δραστηριότητα του συστήματος καλλικρεϊνης-κινίνης και να μειώνει τον αριθμό εμφάνισης αγγειοοιδημάτων. Το φάρμακο χορηγείται υποδορίως κάθε 2-4 εβδομάδες, προσφέροντας βελτίωση στη φροντίδα των ασθενών σε σύγκριση με τις τρέχουσες εναλλακτικές θεραπείες που χορηγούνται είτε ενδοφλεβίως είτε πιο συχνά μέσω υποδόριας οδού. Ως εκ τούτου, η Επιτροπή Φαρμάκων για Ανθρώπινη Χρήση (CHMP) έκρινε ότι το σκεύασμα έχει μεγάλο ενδιαφέρον για τη δημόσια υγεία και συμφώνησε με το αίτημα του αιτούντος για ταχεία αξιολόγηση αυτού του φαρμάκου.
Τα οφέλη και η ασφάλεια του φαρμάκου μελετήθηκαν στη φάση 3 μιας κλινικής μελέτης που αφορούσε 125 ασθενείς. Κατά τη διάρκεια των 26 εβδομάδων θεραπείας, παρατηρήθηκε σημαντική μείωση τόσο στα αγγειοοιδήματα όσο και στην σοβαρότητα που εμφάνιζαν. Οι πιο συχνές ανεπιθύμητες αντιδράσεις ήταν ήπιες και εστιάζονταν στο σημείο της ένεσης.
Επειδή το κληρονομικό αγγειοοίδημα είναι μια πολύ σπάνια ασθένεια η οποία εκτιμάται ότι θα επηρεάσει λιγότερο από 0,5 άτομα σε 10.000 ανθρώπους στην ΕΕ, στο lanadelumab χορηγήθηκε ο χαρακτηρισμός ορφανό, τον Οκτώβριο του 2015.
Προσθέστε το iatronet.gr στο DiscoverΕιδήσεις υγείας σήμερα
Καρκίνος μαστού: Εξέταση αίματος εντοπίζει πρώιμα σημάδια υποτροπής [μελέτη]
Το ''Καρκινάκι’’ σχεδιάζει το Ψηφιακό Σχολείο του Μέλλοντος για μικρούς υπερήρωες
Αυγά και γιαούρτι: Πώς συγκρίνονται σαν πρωινό
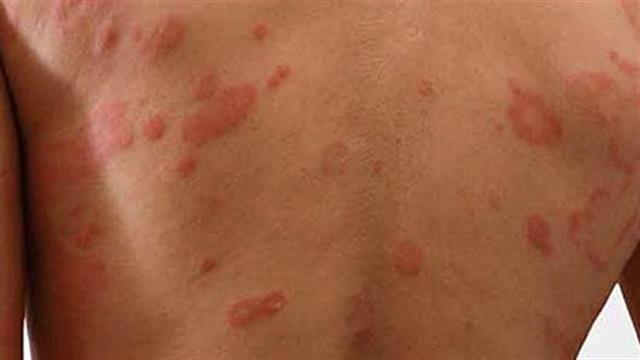
 ‘’Ταυτίζεσαι;’’: Η CSL στο πλευρό των ασθενών με Κληρονομικό Αγγειοοίδημα
‘’Ταυτίζεσαι;’’: Η CSL στο πλευρό των ασθενών με Κληρονομικό Αγγειοοίδημα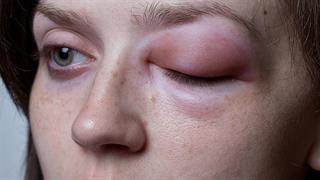 Το donidalorsen έλαβε άδεια κυκλοφορίας στην Ευρωπαϊκή Ένωση για την πρόληψη του κληρονομικού αγγειοοιδήματος
Το donidalorsen έλαβε άδεια κυκλοφορίας στην Ευρωπαϊκή Ένωση για την πρόληψη του κληρονομικού αγγειοοιδήματος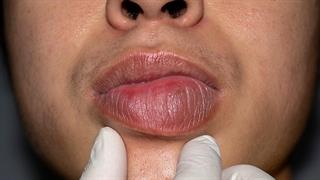 Η CSL Behring παρουσιάζει την εκστρατεία ''Οδύσσεια'' και ρίχνει φως στο κληρονομικό αγγειοοίδημα
Η CSL Behring παρουσιάζει την εκστρατεία ''Οδύσσεια'' και ρίχνει φως στο κληρονομικό αγγειοοίδημα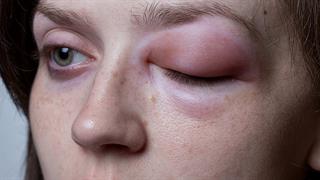 Αυστριακή μελέτη επιβεβαιώνει τη δράση φαρμάκου κατά του αγγειοοιδήματος
Αυστριακή μελέτη επιβεβαιώνει τη δράση φαρμάκου κατά του αγγειοοιδήματος Τι είναι το Κληρονομικό Αγγειοοίδημα και γιατί συχνά συγχέεται με τις αλλεργίες
Τι είναι το Κληρονομικό Αγγειοοίδημα και γιατί συχνά συγχέεται με τις αλλεργίες Κληρονομικό αγγειοοίδημα: Ο αναστολέας της καλλικρεΐνης από το στόμα μειώνει τον αριθμό των επιθέσεων
Κληρονομικό αγγειοοίδημα: Ο αναστολέας της καλλικρεΐνης από το στόμα μειώνει τον αριθμό των επιθέσεων Αυγά και γιαούρτι: Πώς συγκρίνονται σαν πρωινό
Αυγά και γιαούρτι: Πώς συγκρίνονται σαν πρωινό Ορμόνη που συνδέεται με την άσκηση μειώνει συμπτώματα της πολλαπλής σκλήρυνσης [μελέτη]
Ορμόνη που συνδέεται με την άσκηση μειώνει συμπτώματα της πολλαπλής σκλήρυνσης [μελέτη] Πώς αντιλαμβανόμαστε ότι η φωνή προέρχεται από μηχανή και όχι από άνθρωπο (μελέτη)
Πώς αντιλαμβανόμαστε ότι η φωνή προέρχεται από μηχανή και όχι από άνθρωπο (μελέτη) Φορετό επίθεμα υπερήχων θα μπορούσε να βελτιώσει την παρακολούθηση κυήσεων υψηλού κινδύνου
Φορετό επίθεμα υπερήχων θα μπορούσε να βελτιώσει την παρακολούθηση κυήσεων υψηλού κινδύνου 'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία
'Εγκριση της ουσίας μιταπιβάτη στην Ευρωπαϊκή Ένωση για ενήλικες ασθενείς με θαλασσαιμία Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας]
Η Ελλάδα πρώτη σε θανάτους από καρκίνο στην ΕΕ και δεύτερη στον ΟΟΣΑ [πίνακας] Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας
Αντιμετώπιση της παχυσαρκίας: Mια προτεραιότητα της πολιτικής για τη βιωσιμότητα του συστήματος υγείας Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά
Τι αλλάζει για νοσηλευτές-διασώστες η ένταξη στα Βαρέα και Ανθυγιεινά Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς
Απώλεια μυϊκής μάζας με τους αγωνιστές GLP-1 ανησυχεί τους ειδικούς Τι είναι η ALS από την οποία πέθανε ο Παρασκευάς Άντζας στα 49 του
Τι είναι η ALS από την οποία πέθανε ο Παρασκευάς Άντζας στα 49 του Πρωτότυπο φάρμακο ελληνικής προέλευσης; - Πώς θα μπει η χώρα μας στον παγκόσμιο χάρτη
Πρωτότυπο φάρμακο ελληνικής προέλευσης; - Πώς θα μπει η χώρα μας στον παγκόσμιο χάρτη 9 εξακριβωμένα οφέλη του κολοκυθόσπορου
9 εξακριβωμένα οφέλη του κολοκυθόσπορου